ARTRITT (REV 006-REV 020)
32 Psoriasisartritt (PsA) (REV 006)
Psoriasisartritt
Øyvind Palm and Jan Tore Gran
Kjennetegn på psoriasisartritt
Leddsmerter, stivhet og artritt hos personer som har psoriasis.
Hudforandringene (psoriasis) kan være vanskelig å se uten en systematisk vurdering.
Flere subgrupper, inklusiv spondylitt.
Artralgi skilles fra artritt ved klinisk undersøkelse.
CRP og senkningsreaksjon SR er ofte økt, ingen biomarkører/serologiske tester.
Diagnosekoder ICD-10: L40.5 (psoriasis med artropati M07.0- M07.3, M09.0), M07.1 (mutilans, L40.5), M07.2 (psoriasis-spondylitt, L40.5), M07.3 (psoriasisartritt, andre, L40.5), M09 (Juvenil psoriasisartritt), L40 psoriasis (hudsykdom)
Prosedyrekoder: Leddpunksjon/artrocentese (klikk for å spesifisere ledd:) TN_10. UL veiledet leddpunksjon: NXA10K. Mikroskopi av leddvæske: NXFT05.
ATC koder: Behandling med immunsuppressive legemidler: L04A. etanercept: L04AB01, adalimumab: L04AB04, triamcinolon (Lederspan): H02AB08, betametason (Celeston Chronodose): H02AB04, rituksimab: L01XC02, abatacept: L04AA24, tocilizumab: L04AC07, infliksimab: L04AB02, ustekinumab: L04AC05
Definisjon
Psoriasisartritt (PsA) er en inflammatorisk, revmatisk sykdom som består av perifer artritt og/eller spondylitt, entesitt og psoriasis. Sykdommen klassifiseres blant spondyloartritter.
Psoriasis er er en kronisk, inflammatorisk autoimmun hudsykdom som angripe 2-4% av befolkningen, og en genetisk disposisjon er vanlig. Medikamenter som klorokin, litium, betablokkere, kortikosteroider, hydroksyklorokin (Plaquenil) og NSAIDs kan forverre psoriasis, mens soleksponering er gunstig. Psoriasis har mange former / subgrupper: Plakk-psoriasis med sølvgrå skjellende overflate, guttat psoriasis er dråpelignende, pustuløs psoriasis kan være lokalisert (palmoplantaris) eller generalisert, erythroderm psoriasis medfører rødhet og avskalling over store områder, negle-psoriasis har punkter, oljeflekker, hyperkeratose og dystrofi, oral psoriasis tungefissurer, invers psoriasis ses i armhuler, ved mamma, i skrittet og interglutealt som glatt rød, skarpt begrensede hudlesjoner, sebopsoriasis angriper fet hud i hodebunn, panne, bak ører og nasolabialt. Okulær psoriasis ses på øyelokk, konjunktiva og cornea (Nair PA, 2021). -Differensialdiagnoser til psoriasis er eksem, seborreisk dermatitt, pityriasis rosea, mykosis fungoides og sekundær syfilis. -Behandlingen av psoriasis er blitt mye bedre de senere år. Valg av behandlingsform er avhengig av alvorlighetsgraden. Psoriasis Area Severity Index (PASI) er mest brukt for estimering av alvorlighet og for å evaluere behandlingseffekt. Milde-moderate former lokal-behandles blant annet med kremer for huden, mens alvorlige former får systemisk terapi, ofte med metotreksat og biologiske legemidler (Nair PA, 2021).
Historikk
Sammenhengen mellom psoriasis og artritt ble beskrevet av den britiske hudlegen Thomas Batemant i 1813 og i 1818 av den franske hudlegen J.L. Alibert (1768-1837). Benevnelsen psoriasisartritt (PsA) ble foreslått av Pierre Bazin i 1860. Moll & Wright beskrev fem subgrupper av PsA på 50-tallet (Moll JMH, 1973). I 1964 ble PsA skilt fra revmatoid artritt (RA) i ACR-klassifikasjonen av revmatiske sykdommer. Senere er PsA blitt innlemmet i sykdomsgruppen spondyloartritter og klassifisert ved CASPAR-kriteriene (vennligst se nedenfor).
Inndeling av spondyloartritt
- Bekhterevs sykdom/ankyloserende spondylitt
- Psoriasisartritt (spondylitt, polyartritt, oligoartritt, monoartritt)
- Artritt ved kronisk inflammatorisk tarmsykdom (Ulcerøs kolitt, Crohns sykdom)
- Reaktiv artritt
- Udifferensiert spondyloartritt
Sykdomsårsak
Arv er medvirkende. En norsk tvilling-studie viste at 66% av eneggede tvillinger var konkordante for psoriasis og dermed hadde risiko for psoriasisartritt. Samtidig indikerer studien at psoriasis skyldes 34% ikke-genetiske forhold (Grijbovski AM, 2007). HLA-B27 finnes hyppigere ved PsA, særlig ved aksiale manifestasjoner. Ved psoriasis-spondylitt er HLA-B27 sjeldnere (ca. 50%) enn ved Bekhterevs/ankyloserende spondylitt (>95%) og reaktiv artritt. Psoriasisartritt er ikke assosiert med auto-antistoffer slik som ved revmatoid artritt (RA), derimot er PsA er mer T-celle mediert. Det er formulert en alternativ hypotese om at mekanisk stress eller mikroskade i enteser kan initiere en inflammatorisk tilstand og gi PsA (McGonagle D, 2019). En kontrollert studie (case-control design) fant at infeksjoner som krevde antibiotikabehandling, skader og yrker med tunge løft var assosiert med psoriasisartritt, mens det var en invers assosiasjon med røking (Eder L, 2011). Andre har også funnet tegn til at fysisk / mekanisk belastning eller traume kan indusere kan osteofytt-formasjon ved entesitt (dypt Köbner fenomen) (Simon D, 2016).
Epidemiologi
Psoriasis i huden affiserer omkring 2-4% % av befolkningen (prevalens), hvorav ca. 10-30 % med psoriasis får psoriasisartritt (PsA) (Alinaghi F, 2019). Prevalens av psoriasisartritt er i Norge estimert til 0,1-0,2 % (1-2 pr 1.000 personer), uten sikker kjønnsforskjell. Vanlig debutalder er 30-50 år, og sykdommen er vanligst i aldersgruppen 40-59 år (Madland TM, 2005). PsA kan begynne i barnealder (juvenil psoriasisartritt), men er mye sjeldnere enn klassisk barneleddgikt (JIA). Psoriasisartritt utgjør mer enn 50% av alle spondyloartritter (Haglund E, 2010). Mortaliteten synes å være litt økt på grunn av tidlig aterosklerose i noen tilfeller (Fagerli KM, 2018).
Symptomer
Psoriasisartritt kan begynne i det små og være vanskelig å diagnostisere på et tidlig tidspunkt. Det er imidlertid vist at forsinket diagnose med seks måneder fra symptom til første besøk hos revmatolog medfører dårligere prognose ved PsA. Pasientene utvikler flere erosive leddskader, sakroiliitt og redusert fysisk funksjon (Haroon M, 2015).
Hudsymptomene er skjellende erythematøse plakk, oftest på ekstensorsidene av albuer og knær, hos noen også interglutealt, ved umbilicus, palmoplantært og med andre lokalisasjoner. Negler er også ofte angrepet. Psoriasis påvises hos 2-4% i befolkningen (Kurd SK, 2009). Pasienter med utbredt psoriasis (mer enn tre lokalisasjoner) har økt risiko (2,24 x) for PsA (Wilson FC, 2009). Negle pitting og uveitt øker også risikoen (Edel L, 2016). I gjennomsnitt går det 7 år mellom debut av psoriasis og utbrudd av psoriasisartritt, men det er store individuelle variasjoner (Scher JU, 2019). Pustuløs palmoplantar psoriasis er en spesiell form (PPPP-syndrom) som kjennetegnes ved pustuløse hudforandringer i håndflater og fotsåler. Noen skiller fra pustulosis palmoplantaris (PPP-syndrom) som de da ikke regner til psoriasis-subgruppene (Freitas E, 2020).
Artritt ved PsA omfatter mer enn artritt og kan være lett å overse uten målrettet anamnese og undersøkelse. Pasienter med psoriasis bør spørres om leddsmerter, påfallende stivhet i ledd og rygg i mer enn 30 minutter om morgenen (se målrettet anamnese for inflammatorisk ryggsmerte) og tegn til daktylitt.
Moll & Wright beskrev i 1973 fem subklasser av PsA ut i fra mønster av ledd-affeksjon og forløp (Moll JM, 1973) som fortsatt er aktuelle. Subklassene beskriver også aktuelle symptomer fra perifere og aksial ledd.
Inndeling av psoriasisartritt og spondylitt etter Moll JM, 1973
- Artritt med hovedsakelig affeksjon av fingrenes DIP-ledd
- Arthritis mutilans
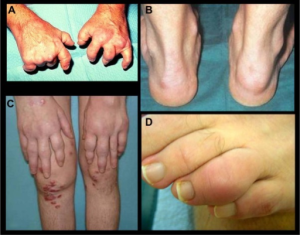
- En sjelden, men alvorlig og karakteristisk tilstand med radiologisk uttalt destruksjon av ledd i hender og føtter (Laasonen L, 2020). Benresorption fører til såkalte “teleskopfingre/-tær” eller “pencil in cup” deformiteter. Ledd-distribusjonen kan være som ved revmatoid artritt. Behandlingen er med NSAIDs, ved inflammasjon også med DMARDs (inklusiv biologiske legemidler), samt revmakirurgi der bedre funksjon kan oppnås
- Oligoartritt
- Etter symmetrisk polyartritt (se nedenfor) den vanligste typen. Færre enn 5 affiserte ledd kan påvises hos 22.9-40%% og monoartritt hos 5,8-15% (Madland TM, 2005; Kasiem FR, 2021). Behandling med leddpunksjon og kortikosteroider i ledd og NSAIDs ved behov. csDMARDs (ofte metotreksat)og biologiske legemidler ved høy sykdomsaktivitet.
- Symmetrisk polyartritt som kan ligne revmatoid artritt, men er negativ for revmatoide faktorer og a-CCP. Behandlingen er som ved revmatoid artritt.
- Den hyppigste subklassen i de fleste studier, og påvist blant 23-68,6% (Madland TM, 2005; Kasiem FR, 2021).
- Spondylitt/aksial artritt
- Iliosakralleddene er angrepet, sjeldnere columna. Isolert spondylitt kan ses hos inntil 2,7% av pasientene med PsA (Madland TM, 2005).
- De radiologiske funnene kan vanligvis skilles fra de man finner ved typisk Bekhterevs/ankyloserende spondylitt. Behandlingen kan være med fysioterapi, NSAIDs og biologiske legemidler ved behov.
I tillegg til denne inndelingen forekommer overlapp mellom disse subklassene og glidning over tid fra mono-/oligoartikulær til polyartikulær artritt og pustuløs palmoplantar psoriasis (PPPP-syndrom) (Freitas E, 2020). En rekke ekstra-artikulære manifestasjoner bør også vurderes i henhold til klassifikasjonskriteriene (vennligst se eget avsnitt nedenfor).
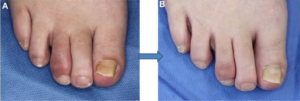
Daktylitt forekomsten ved PsA er ca. 10% ved PsA-diagnose Kasiem FR, 2021) og 40-50% i forløpet. Oftest angripes 3. og 4. tå, men ses også i fingre (Gladman DD, 2013). Illustrasjon: Toshiyuki Yamamoto, 2015, CC BY-NC 3.0
Entesitt er ofte vanskelig å definere, men kan ses hos ca. 10% ved diagnose (Kasiem FR, 2021) og 30-50% i forløpet. Affeksjon av plantarfascien, Akilles-sener, peripatellært, i bekken, epikondylært og ved supraspinatus-senen er vanlig.
Negle-pitting. Forekomsten ved psoriasis er 40%, mens ved psoriasis påvises forandringene hos 80% (Haroon, 2013). En anatomisk likhet mellom negleapparatet og senefester i bensubstans kan være årsaken til en assosiasjon mellom neglepsoriasis og entesopatier ved psoriasis artritt.
Utredning
PsA er en heterogen sykdom med ulik presentasjon. Sykdommen vurderes når det oppstår tegn til artritt eller spondyloartritt hos pasienter med psoriasis. Hudforandringene trenger ikke være uttalt. Diagnosen sikres når andre årsaker er utelukket. I klinisk praksis er legen ikke bundet av å bruke klassifikasjonskriterier for diagnose (se nedenfor). Det er imidlertid vanlig å benytte disse når sykdommen er etablert. Diagnosen PsA kan unntaksvis stilles hos pasienter uten psoriasis forutsatt artritt-sykdommen har karakteristika som PsA, og det er forekomst av psoriasis i nær slekt (se CASPAR-kriteriene nedenfor). Ved utredning av seronegativ artritt er det nyttig å avklare om pasienten har udiagnostisert psoriasis. Sjekk predileksjonsstedene: øregang, hodebunn, navle og negler.
Ved anamnese og klinisk undersøkelse vurderes tidligere og aktuelle symptomer og funn (se ovenfor)
Blodprøver. Rutineprøver kan omfatte CRP, SR, hgb, leukocytter med differensialtellinger, trombocytter,. lever-, nyre- og thyreoidea-funksjonsprøver, anti-CCP og ANA. Urin stiks. CRP og senkningsreaksjon (SR) er forhøyet hos ca. 40%. I forskning er biomarkørene OPG, MMP-3, CPII:C2C ratio (Chandran V, 2010) og CXCL10 (Abji F, 2016) brukt for å skille PsA fra utelukkende hud-manifestasjon. Imidlertid er ingen spesifikke antistoff eller andre biomarkører er tilgjengelig for bruk klinisk hverdag.
Immunologiske tester. Tester for revmatoide faktorer, CCP-antistoff og andre biomarkører forventes å være normale.
Genetikk. HLA-B27 foreligger hos ca. 50% med aksial affeksjon som er sjeldnere enn ved Bekhterevs (ca. 95%) og ved IBD-relatert spondyloartritt (ca. 75%). HLA allelene B*08, B*27 og B*38 er risikofaktorer for utvikling av PsA, mens HLA-C*06 er beskyttende (Eder L, 2012). Disse testene er imidlertid ikke tilgjengelig for bruk i klinisk hverdag. Se også sykdomsårsaker ovenfor.
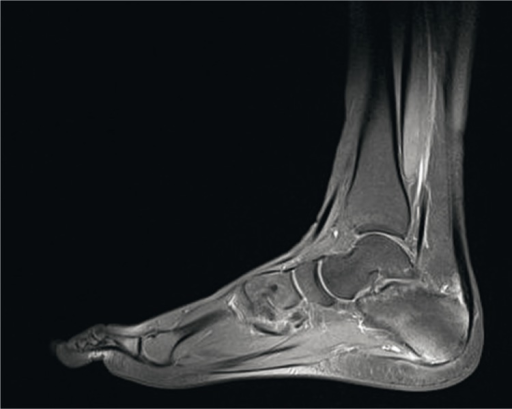
Bildediagnostikk. Artritt i perifere ledd påvises ved klinisk undersøkelse, eventuelt supplert med ultralyd eller MR. Radiografisk er tegn på ben- og bruskdestruksjon slik som smal leddspalte, erosjoner og ny benformasjon i form av periostitt, osteofytter (forkalkninger) ved senefester (entesofytter) og benet ankylose. Aksial affeksjon påvises bildediagnostisk med røntgen-, CT- eller MR-undersøkelser som ved Bekhterevs/ankyloserende spondylitt. Sammenlignet med Bekhterevs ses unilateral sakroiliitt hyppigere ved PsA. Ultralyd Doppler kan påvise tendinitt og tenosynovitt ved daktylitt og tegn til inflammasjon ved entesopati. Illustrasjon (MR): Sudoł-Szopińska I, Kwiatkowska B, Prochorec-Sobieszek M, Pracoń G, Walentowska-Janowicz M, Maśliński W – Journal of ultrasonography (2015). CC BY-NC-ND 3.0.
Klassifikasjonskriterier
Klassifikasjonskriterier for PsA er ikke validert, men brukes som retningslinjer i klinisk praksis og i forskning. Selv om CASPAR kriteriene ble basert på pasienter med langvarig sykdom, er det vist at de også fungerer godt i tidlig sykdomsfase (Chandran V, 2007).
| Klassifikasjonskriterier for psoriasisartritt (CASPAR) krever perifer eller aksial artritt eller entesitt og 3 eller flere poeng/Score fra følgende 5 punkter: |
||
| Kriterium | Forklaring | Score |
| 1. Forekomst av psoriasis | ||
| -Nåværende Psoriasis | Psoriasis i huden eller hodebunnen påvist av dermatolog eller revmatolog | 2 |
| -Sykehistorie på psoriasis | Anamnese i henhold til pasient, fastlege, hudlege eller revmatolog | 1 |
| -Familie-anamnese på psoriasis | Psoriasis hos første- eller andregrads slektninger i henhold til pasientens opplysninger | 1 |
| 2. Psoriasis i negler (negle-dystrofi) | Typisk negle-dystrofi (onycholyse, pitting, hyperkeratose) observert av lege ved aktuell konsultasjon | 1 |
| 3. Negativ test for revmafaktorer | Gjelder ikke latex-test, ellers alle revmafaktor tester, fortrinnsvis ELISA eller nefelometri. Utslag over referanseområdene | 1 |
| 4. Daktylitt | ||
| -Pågående daktylitt | Hevelse i hele finger/tås lengde som observeres ved legeundersøkelsen | 1 |
| -Sykehistorie på daktylitt | I henhold til revmatolog | 1 |
| 5. Radiografisk påvist juksta-artikulær ny benformasjon | Patologisk ossifikasjon nær leddspaltene (ikke osteofytter) ved røntgen av hender eller føtter | |
| 98,7% spesifisitet og 91,4% sensitivitet, Taylor W, 2006 | ||
Differensialdiagnoser
PsA må skilles fra andre former for spondyloartritt, revmatoid artritt (RA), artrose, urinsyregikt og systemisk lupus (SLE). Også pustulosis palmoplantaris og SAPHO syndromet kan vurderes.
| Psoriasis-artritt til forskjell fra revmatoid artritt (RA): Tabell tilpasset etter Coates LC, Clinical Medicine 2017: |
||
| Symptomer | PsA | RA |
| Antall affiserte ledd | 30-50% har oligoartritt | Polyartritt vanligst |
| Ledd-affeksjon | Hvilket som helst, inkludert DIP | Ikke DIP ledd |
| Entesitt | Klinisk hos 60-80% | Uvanlig |
| Daktylitt | Klinisk hos 30% | Uvanlig |
| Aksial affeksjon | Aksial fenotype | Erosiv cervikal affeksjon |
| Kutan/negle affeksjon | Psoriasis: 80% hud, 60% negler | Ikke økt forekomst |
| Serologiske antistoff | RF og CCP vanligvis negative | RF og CCP oftest positive |
| Bildediagnostikk | Periostal ny benformasjon | Erosjoner og osteopeni |
| Forskjeller på ulike spondyloartritter (Richlin CT, 2018) | ||||
| Kjennetegn | Psoriasisartritt | Bekhterevs /ankyloserende spondylitt | Reaktiv artritt | IBD-assosiert artritt |
| Alder ved debut (år) | 36 | 20 | 30 | 30 |
| Mann/kvinne ratio | 1:1 | 3:1 | 3:1 | 2:1 |
| Perifer artritt | 96% | 30% | 90% | 30% |
| Aksial artritt | 50% | 100% | – | 30% |
| Daktylitt | Vanlig | Fraværende | Uvanlig | Fraværende |
| Entesitt | Vanlig | vanlig | Uvanlig | Uvanlig |
| Psoriasis | 100% | 10% | 10% | 10% |
| Negle-lesjoner | 87% | Uvanlig | Uvanlig | Uvanlig |
| HLA-B27 | 40-50% | 90% | 70% | 30% |
Komorbiditet
Ved PsA er det økt forekomst av kardiovaskulære risikofaktorer som adipositas, hyper/dyslipidemi, diabetes type 2, hypertensjon og fysisk inaktivitet. Identifisering og behandling av risikofaktorer bør gjøres i samarbeid med fastlege. Uveitt ses hos 8%.
Sykdoms-score
- Senkningsreaksjon (SR) og CRP korrelerer med inflammatorisk aktivitet, men i mindre grad enn ved RA.
- Perifer artritt: 28-Ieddstatus brukes ofte, men pga. hyppig affeksjon av DIP- ledd, føtter og ankler bør disse også undersøkes.
- BASDAI (Bath ankylosing spondylitis activity index) anvendes i klinisk praksis også ved monitorering av aksial PsA.
- Et sammensatt sykdoms-score er foreslått: CPDAI (composite psoriatic disease activity index).
- Ultralyd er nyttig til å diagnostisere og monitorere entesitt, daktylitt og perifer artritt.
- Utbredelse av psoriasis i huden estimeres ved PASI score
- Ved polyartritt kan røntgen av hender/håndledd og føtter benyttes til artritt-klassifikasjon (jfr. CASPAR) og monitorering.
Vennligst se også kapittel om kliniske verktøy og skåringssystemer
Svangerskap
Litt over halvparten (53%) av pasienter med psoriasisartritt opplever lavere sykdomsaktivitet under svangerskap, men omtrent 40% får sykdomsresidiv i ukene etter fødsel (Østensen M, 1988; (Polachek A., Li S 2017). Data fra den norske REVNATUS studien bekreftet lavere sykdomsaktivitet i svangerskap og noe høyere sykdomsaktivitet 6 måneder post partum (Ursin K, 2019). Blant pasienter med høy sykdomsaktivitet er det aktuelt å vurdere om behandlingen kan kontinueres gjennom den første 2/3 delen av svangerskapet, unntaksvis under hele graviditeten. Det gjelder imidlertid ikke for alle medikamenter. Blant andre må metotreksat seponeres før svangerskap. Sammenlignet med gravide uten psoriasisartritt foreligger litt økt risiko for tidlig fødsel (OR 1,63) og for keisersnitt (OR1,47-1,43), men ikke økt risiko for spontanaborter, dødfødsler eller misdannelser (Remaeus K, 2019). Psoriasis i huden blir bedre eller uendret hos over 80% i løpet av svangerskap (Berman M, 2018). Vennligst se mer i eget kapittel om svangerskap og info fra NKSR.
Behandling
Behandlingen ved PsA bør person-tilpasses i stor grad fordi sykdommen er svært heterogen. En bør før behandlingsstart vurdere hvilke manifestasjoner som foreligger (perifer artritt, aksial sykdom, daktylitt, entesitt, psoriasis og negle-sykdom), og hvilke av disse som for pasienten er viktigst å behandle. Selv om behandlings-strategier med tidlig oppstart og “treat to target” er varierende dokumentert ved PsA, er det viktig for prognosen og behandlingsresultatet å behandle mot et på forhånd fastsatt mål og begynne tidlig når det er nødvendig. Behandlingsmål som vektlegges ved PsA er minimal eller ingen sykdomsaktivitet/inflammasjon, optimal fysisk funksjon, bedre livskvalitet og sosial deltakelse, forhindre strukturell skade og minimalisere komplikasjoner av behandlingen (Coates LC, 2016). Suppresjon av inflammasjon er viktig for å kunne nå disse målene (Gossec L, 2020). Vurdering av sykdomsaktiviteten initialt og registrering av denne i forløpet er da nyttig. I motsetning til kutan behandling av mange med utelukkende hud-psoriasis, behandles psoriasisartritt oftest med systemisk virkende medikasjon.
NSAIDs er symptomatisk basisbehandling og kan være tilstrekkelig ved mild artritt.
Steroid-leddinjeksjoner kan være særlig nyttig ved mono- og oligoartritt.
csDMARDs. Vedvarende perifer artritt kan behandles med csDMARDs som metotreksat eller leflunomid (Arava), ev. sulfasalazin, eller ciclosporin A (Sandimmun). Metotreksat foretrekkes derom også hud-manifestasjon trenger behandling. Kombinasjon av metotreksat og TNF-hemmer brukes ofte dersom metotreksat alene ikke er tilstrekkelig (Fagerli MK, 2012). Ikke alle DMARDs har PsA som godkjent indikasjon. Når medikamenter brukes utenfor godkjent indikasjon skal en informere og dokumentere spesielt grundig (vennligst se eget kapittel om utprøvende behandling).
Apremilast (Otezla) har vist effekt ved psoriasisartritt og brukes som alternativ når TNF-hemmere og annen biologisk medikasjon ikke har effekt eller ikke kan brukes av andre årsaker. Medikamentet er gunstig bivirkningsprofil (Reed M, 2017), men høy kostand gjør at det ikke er i bruk i Norge (pr 2023).
Biologiske legemidler (bDMARDs). Ved utilstrekkelig effekt av minst ett DMARDs kan biologisk behandling være indisert. TNF-hemmer er ofte første-valget. TNF-hemmere har vist god effekt også over lengre sykdomsforløp (Fagerli KM, 2018). Secukinumab (Cosentyx) en Interleukin-17A-Inhibitor eller ustekinumab (Stellara) en IL-12 /-23 hemmer er alternativer, oftest dersom TNF-hemmere ikke er aktuelle.
JAK-hemmere (tsDMARDs) som Tofacitinib (Xelans) og Baricitinib (Olumiant) har også vist effekt og brukes for eksempel dersom DMARDs og minst ett biologisk legemiddel ikke har tilstrekkelig effekt.
Spondylitt og entesitt behandles ofte som ved Bekhterevs/ankyloserende spondylitt med NSAIDs, fysioterapi og/eller biologisk legemiddel som TNF- hemmer eller IL-17 hemmer (Secukinumab).
Ved stabil remisjon vurderes om sykdomsdempende behandlingen kan trappes ned.
Prednisolon unngås så langt som mulig ved PsA fordi nedtrapping/seponering kan medføre eksaserbasjon av psoriasis (rebound fenomen). Eksaserbasjon av psoriasis i huden ses også ved bruk av hydroksyklorokin (Plaquenil) som vanligvis ikke er anbefalt.
Prognose
Psoriasisartritt må oppfattes som en alvorlig form for artritt. Studier før biologisk behandling viser at 47% utviklet erosjoner i ledd i løpet av de første to år til tross for DMARDs (Kane D, 2003). Sykdommen forløper imidlertid fredeligere under behandling med biologiske legemidler, men residiv ved seponering må forventes. Spontan remisjon er svært uvanlig. Perifer artritt forløper variabelt fra selvbegrensende/ikke-destruktiv via langsomt progredierende til uttalt destruktive forløp. Prediktorer for destruktivt forløp er polyartritt, høy SR/CRP, daktylitt og/eller negle-manifestasjoner, terapiresistens og allerede påvist leddskade. Det er rapportert økt risiko for kardiovaskulær sykdom med koronararterie-manifestasjoner ved PsA, noe som bidrar til at mortaliteten er økt sammenlignet med den generelle befolkningen (Fagerli KM, 2018).
Retningslinjer, anbefalinger og prosedyrer
EULAR: Gossec L, 2020 (medikamenter)
GRAPPA/EULAR 2017, Coates LC, 2017
Norsk Revmatologisk Forening/Legeforeningen
- Vennligst les mer om behandlingsretningslinjer i eget kapittel
