VASKULITT (REV 034-052)
85 Cogans syndrom (REV 036)
Cogans Syndrom
Ragnar Gunnarsson
Kjennetegn på Cogans syndrom
Svært sjelden autoimmun kronisk betennelsessykdom.
Inflammatorisk øyesykdom, som oftest interstitial keratitt sammen med hørsel og/eller vestibulære manifestasjoner.
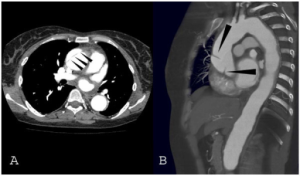
Vaskulittforandringer påvises i opp til 20% tilfelle og da oftest i aorta.
Oftest økt inflammasjonsparametre i blodprøver (C-reaktiv protein og senkning).
Assosiert til anti-Hsp70 («Heat shock protein 70») antistoff.
Diagnosekoder ICD-10: M31.8, vaskulitt, annen. H91.8 Annet uspesifisert hørselstap; H20.0 Uveitt, iridocyklitt
ATC koder (for legemiddelstatistikk): Prednisolon: H02A B06 Immunsuppressive legemidler: L04A A
Definisjon
Cogans syndrom (CS) er en svært sjelden autoimmun kronisk betennelsessykdom som affiserer øye, med som oftest interstitial keratitt, mellomøre og bevegelsesapparat med vestibulo-auditiv dysfunksjon og kar med vaskulitt.
Historikk
Morgan og Baumgartner beskrevet i 1934 pasient med Ménières sykdom og interstitial keratitt (1). Elleve år senere beskrev øyelegen David G. Cogan fra Boston USA, fire pasienter med kombinasjonen av interstitial keratitt og vestibuloauditiv dysfunksjon som liknet på Ménières sykdom (2).
Epidemiologi
Det foreligger ingen epidemiologiske data på CS men tilstanden er sjelden. CS ser ut til å ramme helst unge voksne, dvs. de mellom 20-40 år og ut fra publiserte rapporter virker det som lik kjønnsdeling. Det er noe over 300 publiserte tilfeller (3-6). Det foreligger ingen sikre tall om insidens eller prevalens av tilstanden. Det har vært publisert en rekke pasientkohorter de to største er fra Frankrike med 40 pasienter og innhentet informasjon om 22 pasienter i tillegg (6), men største enkelte pasientkohort ble publisert i 2006 fra Mayo Clinic i Rochester USA med 60 pasienter som ble følget opp fra 1940-2002 (5).
Patogenese og patologi
Det foreligger begrenset histologimateriale fra pasienter med CS. Det foreligger per dags dato ingen histologiske bevis for at det foreligger vaskulitt i det indre øre eller øye. Histologi fra øyens hornhinne av pasienter med interstitiell keratitt, har vist infiltrasjon av lymfocytter og plasmaceller i dypere lager av hornhinne.
Patogenese er ukjent, men mye tyder på at sykdommen er autoimmune og det er også tegn som kan tyde på at den kan være infeksjonsutløst. Det har vært funnet sammenheng med spesifikke autoantistoff assosiert til tilstanden. Disse antistoff har likhet med Ro/SSA autoantigenet, og innbefatter antistoffer mot density enhanced protein tyrosine phosphatase-1 (DEP-1/CD148), connexin 26 og reovirus III-hovedkjerneprotein lambda 1 (7). Det styrker hypotesen at man klart å reprodusere sykdommen i dyreforsøk på mus med overføring av autoantistoffet som reagere på antigen i det indre øre. Det har også vært funnet sammenheng ved klassisk form av CS og et antistoffer mot et 68 kDa-antigen som er identifisert som «heat shock protein 70» (Hsp70). Anti-Hsp70-antistoffer ble funnet på varierende nivåer hos pasienter som presenterer forskjellige former for autoimmunt sensorineuralt hørselstap inklusiv klassisk form av CS der 93% (13/14) hadde påvist antistoffet versus 17% (4/24) med det som var definert som atypisk form av CS (8). I Mayo Clinic kohort undersøkelsen hadde kun 10% anti-Hsp70 antistoff og man fant ingen sammenheng med sykdomsutvikling (5).
Kriterier for klassifikasjon og mål på sykdomsaktivitet
Det finnes ingen validerte diagnostiske eller klassifikasjonskriteria for CS.
Klinikk
Diagnosen CS baserer seg på mønstergjenkjenning der pasienten utvikler symptomer øye og audiovestibular sykdom. Forut dette utvikler pasienten som oftest allmenn symptomer i 70-80% tilfelle. Symptomer som feber, vekttap og utmattelse. Det er rapporter om at omtrent 10% har underliggende autoimmun sykdom som; reumatoid artritt, spondyloartritt, inflammatorisk tarmsykdom, sarkoidose, autoimmune thyreoida-sykdommer, relapsing polykondritt, TINU syndrom (tubulointerstitiell nefritt og uveitt), ANCA assosierte vaskulitter (AAV), Takayasus arteritt og polyarteritis nodosa (9). Pasienter med CS kommer i hovedsak fra spesialister i ØNH og oftalmologi.
Øyesymptomer er vanligvis bilaterale og er oftest interstitiell keratitt (IK) med smertefullt rødt øye, lysømfintlighet og tåkesyn. Sjeldnere kan det oppstå konjunktivitt, iridocyklitt, skleritt eller episkleritt men andre sjeldnere øyemanifestasjon har vært beskrevet deriblant retinal vaskulitt. Øyemanifestasjonene kan komme akutt og ledsaget av smerte og fotofobi. De kan også fluktuere. Det er viktig med øyelegeundersøkelse og oppfølging. Spaltelampeundersøkelse påvises ofte spredte infiltrater i kornea.
Audiovestibular symptomer oppstår vanligvis plutselig og er som oftest unilateral ved debut. Det kan manifestere seg som akutt innsettende svimmelhet, kvalme og oppkast, ataksi, nystagmus og øresus og hørselstap. Dette kan minne på anfall ved Ménère sykdom.
Vaskulitt påvises i 15-20% tilfeller av CS, derav aortitt hos totalt ca. 10%. Også koronar arteritt er rapportert. I Mayo Clinic kohorten var referert at 8/60 13% hadde vaskulitt (5).
Differensialdiagnoser ved Cogans sykdom
Sarkoidose, Behçets syndrom, polyarteritis nodosa (PAN), Takayasus arteritt, granulomatose med polyangiitt (GPA), relapserende polykondritt, systemisk lupus erytematosus (SLE), revmatoid artritt (RA), Crohns sykdom og IgG4 assosiert sykdom. Vogt-Koyanagi-Harada syndrom, Méninères sykdom, Syfilis, borreliose/Lyme sykdom, tuberkulose, HIV, bakteriell endokarditt samt lokalisert infeksjoner som forårsaker viral eller bakteriell keratitt. I tillegg vaskulære hendelser eller tumorer i som bl.a. kan affiserer cerebellopontin vinkelen.
Undersøkelser
Diagnosen er svært sjelden og utredning krever omfattende kartlegging og eksklusjon av aktuelle differensialdiagnoser.
Oftalmologi: Kartlegging av øyelege med spaltelampe, prøvetakning i henhold til bakteriell/viral årsak for keratitt. I tillegg kartlegging av syn og synsfelter, samt fundoskopi med bilder og evt. fluorescein angiografi.
Øre-nese-hals lege (ØNH): Kartlegging med audiogram og caloric reflex test.
Blodprøver: I tillegg til utvidet hematologisk status, lever- og nyrefunksjonsparametere samt elektrolytter inklusivt serum kalsium og fritt kalsium. Inflammasjonsparametere som C-reaktiv protein (CRP) og senkning (SR). Autoantistoffer som revmafaktor, anti-CCP og anti-nukleære antistoffer (ANA). Anti-neutrofilt cytoplasmatisk antistoffer (ANCA/MPO/PR3) samt IgG subklasse inkl. IgG4 analyse. Antifosfolipid antistoffer, Lupus antikoagulans og komplement analyse for bl.a. komplementfaktorer C3, C4. Serologiske prøver for syfilis, Borrelia burgdorferi, virale hepatitter og «Human Immune Deficiency Virus» (HIV) og Mycobacterium tuberculosis med for eksempel. TB-IGRA QuantiFeron (IGRA – interferon gamma release assay). Andre undersøkelser kan vurderes som oppløselig IL-2 reseptor og angiotensinkonverterende enzym (ACE) for sarkoidose diagnostikk. Man kan vurdere å ta anti-Hsp70 («Heat shock protein 70») som tas ved autoimmun hørselstap. Anti-Hsp70 analyseres foreløpig ikke Norge, men på Wieslab AB i Sverige som immunblot der resultat angis som enten positivt eller negativt. WIESLAB Diagnostic Services, Wieslab AB, Lundavägen 151 SE-21224 Malmö, Sweden.
Radiologiske undersøkelser: Magnetisk resonans bildediagnostikk (MRI) ofte med angiografi (MRA) av cerebrum og hjernestamme som inkluderer mellomøre og cerebellopontin vinkelen. Dette kan påvise væskesignal med labyrintitt eller forkalkning. MR-Angiografi av aorta kan verifisere aortitt eller arteritt i store kar.
18FDG PET/CT/MRI undersøkelse. En positronemisjonstomografi (PET) med radioaktivt sporstoff, som oftest er 18fluor merket sammen med deoksyglukose som er en druesukkerforbindelse. PET er oftest knyttet opp til MRI eller computer tomografi (CT). Det er aktuelt å utføre PET sann hvis det er spørsmål om vaskulitt i store kar samt for å utelukke aktuelle differensiell diagnoser som; sarkoidose, IgG4 assosiert sykdom og tuberkulose bl.a.
Andre undersøkelser bør vurderes som spinalpunksjon og nevrologisk vurdering og eventuelt elektroencefalograf (EEG) og «somatosensory evoked potentials» (SEP) undersøkelser.
Ekkokardiografi (EKKO-cor) bør vurderes der det er rapporter på hjerteklaffeaffeksjon ved CS særlig hos de med affeksjon av aorta ascendens og bakteriell endokarditt kan være en differensial diagnose.
Behandling
Det foreligger ingen randomiserte studier på behandlingseffekt og det foreligger ingen internasjonale anbefalinger om behandling. Generelt er glukokortikoid (GC) brukt og lokal steroid behandling har bra dokumentert effekt på keratitt og anterior uveitt mens bakre uveitt og retinitt krever systemisk GC behandling.
Kortikosteroider. Ved audiovestibular symptomer som akutt innsettende hørselstap vil fleste bruke høydose (1-2mg/daglig) per oral Prednisolon der man vanligvis ikke overstiger det som tilsvarer 60 mg/døgnet. Innledningsvis. Ved alvorlig affeksjon kan evt. intravenøs metylprednisolon (125 – 1.000 mg daglig) da over tre dager og etterfulgt av per oral høy prednisolon behandling som skissert. De pasientene som har refraktær sykdom, må man legge opp til langvarig steroid behandling og vil man prøve å gi steroid sparende behandling. Der har vi dessverre ingen prospektive randomiserte studier og den medisinske litteratur baseres på retrospektive kasuistikker og historiske pasientkohorter med antatt betydelig publikasjonsbias på effekt.
DMARDs. Fleste velger først per oral eller subkutant metotreksat (MTX) 15-25 mg/uke, som steroid sparende medikament. Alternativt kan man vurdere azathioprin (AZA)/Imurel rundt 2 mg/kg per dag. Det foreligger rapporter på per oral cyklofosfamid behandling, mykofenolat og på kalsineurin hammerne; ciclosporin og takrolimus.
Biologiske legemidler. Det er flerre rapporter om positiv effekt av anti-TNFα behandling, der det kun har vist effekt av antistoffer i hovedsak infliksimab (6), men etanercept har ikke vist seg å være virksomt hi en prospektiv studie på immunrelaterte cochlea-vestibular lidelser (IMCVDs) (10). Det foreligger enkeltstående rapporter på effekt og manglende effekt av rituksimab (RTX) (anti-CD20 antistoff) og kasuistikk på effekt av tocilizumab (anti-Interleukin-6 antistoff) (11-13).
Per dags dato vil man igangsette steroid behandling og legge til MTX hvis intoleranse vurdere AZA og hvis utilstrekkelig effekt forsøke først med intravenøst infliksimab (anti-TNF-alfa antistoff) som tertier behandling.
Prognose
Sykdomsforløp ved CS karakterers av tilbakefall. I CS kohorten fra Mayo Clinic (60 pasienter) var rapportert om at 62% av pasientene hadde rekke tilbakefall mens 13% hadde ett isolert tilbakefall, mens 2 pasienter (3%) kom aldri i remisjon (5). Nyere oppfølging fra en fransk kohort undersøkelse (62 pasienter) der bruk av langvarig immunsuppressiv behandling var mer uttalt, viste 13% tilbakefall etter 5 år og 31% tilbakefall etter 10 år.
Øyeaffeksjonen har som regel god prognose mens særlig affeksjon på hørsel har dårlig prognose og fleste pasienter har sekvele i form av permanent hørselssvekkelse og øresus.
Litteratur
Referanser
- RF M, CF B. Menier’s disease complicated by recurrent interstitial keratitis. Excellent result following cervial ganglionectomy. West J Surg. 1934;42:628.
- DA C. Syndrome of nonsyphilitic interstitial keratitis and vestibuloauditory symptoms. Arch Ophthalmol. 1945;33:144-9.
- Haynes BF, Kaiser-Kupfer MI, Mason P, Fauci AS. Cogan syndrome: studies in thirteen patients, long-term follow-up, and a review of the literature. Medicine (Baltimore). 1980 Nov;59(6):426-41. PubMed PMID: 6969345.
- Grasland A, Pouchot J, Hachulla E, Blétry O, Papo T, Vinceneux P. Typical and atypical Cogan’s syndrome: 32 cases and review of the literature. Rheumatology (Oxford). 2004 Aug;43(8):1007-15. PubMed PMID: 15150435.
- Gluth MB, Baratz KH, Matteson EL, Driscoll CL. Cogan syndrome: a retrospective review of 60 patients throughout a half century. Mayo Clin Proc. 2006 Apr;81(4):483-8. PubMed PMID: 16610568.
- Durtette C, Hachulla E, Resche-Rigon M, Papo T, Zénone T, Lioger B, et al. Cogan syndrome: Characteristics, outcome and treatment in a French nationwide retrospective study and literature review. Autoimmun Rev. 2017 Dec;16(12):1219-23. PubMed PMID: 29037902.
- Lunardi C, Bason C, Leandri M, Navone R, Lestani M, Millo E, et al. Autoantibodies to inner ear and endothelial antigens in Cogan’s syndrome. Lancet. 2002 Sep 21;360(9337):915-21. PubMed PMID: 12354474.
- Bonaguri C, Orsoni J, Russo A, Rubino P, Bacciu S, Lippi G, et al. Cogan’s syndrome: anti-Hsp70 antibodies are a serological marker in the typical form. Isr Med Assoc J. 2014 May;16(5):285-8. PubMed PMID: 24979832.
- Espinoza GM, Wheeler J, Temprano KK, Keller AP. Cogan’s Syndrome: Clinical Presentations and Update on Treatment. Curr Allergy Asthma Rep. 2020 Jun 16;20(9):46. PubMed PMID: 32548646.
- Matteson EL, Choi HK, Poe DS, Wise C, Lowe VJ, McDonald TJ, et al. Etanercept therapy for immune-mediated cochleovestibular disorders: a multi-center, open-label, pilot study. Arthritis Rheum. 2005 Jun 15;53(3):337-42. PubMed PMID: 15934127.
- Shibuya M, Fujio K, Morita K, Harada H, Kanda H, Yamamoto K. Successful treatment with tocilizumab in a case of Cogan’s syndrome complicated with aortitis. Mod Rheumatol. 2013 May;23(3):577-81. PubMed PMID: 22752533.
- Bunker DR, Kerr LD. Rituximab Not Effective for Hearing Loss in Cogan’s Syndrome. Case reports in rheumatology. 2016;2016:8352893. PubMed PMID: 27843668. PMCID: PMC5098068.
- Orsoni JG, Laganà B, Rubino P, Zavota L, Bacciu S, Mora P. Rituximab ameliorated severe hearing loss in Cogan’s syndrome: a case report. Orphanet journal of rare diseases. 2010;5:18-. PubMed PMID: 20550723.
