VASKULITT (REV 034-052)
81 Arteritis Temporalis (AT) / Temporalis arteritt / Kjempecellearteritt (GCA) og ekstrakranial/non-kranial storkarsvaskulitt (REV 034)
Jan Tore Gran and Øyvind Palm
Kjennetegn på temporalis arteritt og ekstrakranial storkarsvaskulitt
Alle er over 50 år, de fleste også over 65 års alder.
Tydelig forhøyet CRP og SR
Tinning-hodepine er ikke alltid til stede, selv om temporal arterien er affisert.
Non-kranial storkarsvaskulitt kjennetegnes ved noe lavere alder, flere kvinner, diffuse eller ingen åpenbare vaskulitt-symptomer (“silent vasculitis”) og lengre latenstid før diagnose enn ved arteritis temporalis.
Polymyalgia revmatika kan forekommer samtidig både med og uten temporalarterie-affeksjon.
Ultralyd, CT eller PET/CT viser ev tegn på vaskulitt i store arterier.
Diagnosekoder ICD-10:: M31.6 (uten polymyalgia), M31.5 med polymyalgia. M31.9 Uspesifisert nekrotiserende vaskulitt
Prosedyrer: EKG: FPFE15
ATC koder (for legemiddelstatistikk): Prednisolon: H02A B06 Immunsuppressive legemidler: L04A A
Definisjon
Arteritis temporalis (AT) / temporal arteritis er en vaskulitt-sykdom som angriper personer over 50 års alder. Sykdommen kjennetegnes av inflammasjon i kraniale arterier, særlig i tinninger (temporalis-arteriene) og bakhodet (occipitalis-arteriene). Blodforsyning til øyne (risiko for blindhet), kjevemuskler (tyggeklaudikasjon) og skalpen (skalpsmerter/nekrose) kan påvirkes. Temporalis arteritt angriper også store arterier (storkarsvaskulitt) som aorta, a. carotis, a. subclavia og a. brachialis i opp til 100% av pasientene basert på funn ved PET/CT og ved autopsier (Gribbons KB, 2020). Nær halvparten av pasientene får også raskt innsettende muskelsmerter i form av polymyalgia revmatika (PMR) (Pugh D, 2022).
Ekstrakranial (non-kranial) storkarsvaskulitt ligner arteritis temporalis, men kraniale arterier angripes ikke (vennligst se mer nedenfor), noe som gjør den vanskeligere å gjenkjenne. Typisk er systemisk inflammasjon hos eldre personer, men uten spesifikke organfunn (“silent vasculitis”). Ekstrakranial storkarsvaskulitt bør således mistenkes blant eldre med uklart forhøyede inflammasjonsparametere kombinert med enten uspesifikke symptomer eller tegn på perifer arteriell sykdom som ikke skyldes aterosklerose (Lensen KDF, 2016).
Juvenil arteritis temporalis er en sjelden annen sykdom som medfører fortykket arteria temporalis hos unge personer (Kolman OK, 2009). Vennligst se mer under “Spesielle sykdomsgrupper” nedenfor.
Både klassisk temporalis arteritt og ekstrakranial storkarsvaskulitt kalles kjempecelle-arteritt (engelsk: giant cell arteritis, GCA), fordi en histologisk kan finne kjempeceller ved histologisk undersøkelse. Sykdommene klassifiseres blant vaskulitter i store kar (storkarsvaskulitt) sammen med Takayasus arteritt, Cogans syndrom og isolert aortitt.
Historikk
Muligens er den første dokumentasjonen av arteritis temporalis (AT) og polymyalgia revmatika (PMR) å finne i Jan van Eycks (1385-1440) maleri “The Holy Virgin with Canon van der Paele” (1436, Brugge Gemeenter museum), hvor venstre temporalarterie prominerer betydelig (vennligst se illustrasjonen nedenfor). Etter sigende skulle han også ha hatt vansker med å forrette morgengudstjenesten på grunn av generell stivhet og nedsatt allmenntilstand. Sir Jonathan Hutchinson (1828-1913) (London) beskrev AT i 1890 (“thrombotic arteritis of the aged”) (Pearce JM, 1994). De histologiske forandringene ble beskrevet av Bayard T. Horton (1895-1980) ved Mayo klinikken 7. desember 1932 (Horton BT, 1946). Insidensen av temporalis arteritt i Norge ble første gang estimert i Aust-Agder (Gran JT, 1997).
Epidemiologi
Årlig insidens av AT per 100.000 innbyggere 50 år eller eldre varierer fra 5,1-33,6. I Norge er den beregnet til 20,7-29/100.000 i aldersgruppen 50 år og eldre og 8-9/100.000 i hele befolkningen (Gran JT, 1997; Skaug HK, 2023). Forekomst av ekstrakranial manifestasjon ved arteritis temporalis var tidligere estimert til 3-15% (Klein RG 1975), men en autopsistudie påviste hele 92% (Östberg G, 1973). Med nyere bildediagnostiske metoder som omfatter PET/CT er det funnet at opp til 83% med AT har ekstrakranial storkarsvaskulitt (Blockmans D, 2006). Sykdommen er mye vanligere blant etnisk skandinaviere enn personer av Sør-Europeisk, Asiatisk eller Afrikansk opphav (Watts RA, 2022).
Ekstrakranial storkarsvaskulitt. Det er ikke gjort epidemiologiske studier på uspesifisert ekstrakranial storkarsvaskulitt, men forekomsten kan være høyere enn for arteritis temporalis (Lensen KDF, 2016).
Etiologi
Sykdomsårsaken ved arteritis temporalis er ikke avklart. Genetiske forhold spiller en rolle. Single nukleotid polymorfisme (SNPs) i HLA klasse II gen-regioner og sørlig i området mellom HLA-DRA og HLADRB1 er assosiert med arteritis temporalis (Carmona FD, 2015). Risiko for arteritis temporalis blant første grad slekt er noe økt (SIR 2,14). Der et også funnet noe økt forekomst av andre autoimmune sykdommer blant 1. grads slekt (PMR, primær biliær kolangitt, psoriasis, RA, Sjøgrens) (Thomsen H, 2020). Til forskjell fra mange livsstilsykdommer er det funnet at temporalis arteritt er assosiert med lav glukose, lave triglyserider, lav kolesterol og lav BMI (Jacobsson K, 2015). Juvenil arteritis temporalis har en annen etiologi og patogenese (Pipinos II, 2006).
Patogenese
Temporalis arteritt er en autoimmun sykdom i medium- og store arterier. Den kjennetegnes ved granulomatøs inflammasjon i alle tre lag av arterieveggene, noe som resulterer i stenoser, okklusjoner, disseksjoner og aneurismer. Immunpatogenesen er en akkumulerende prosess som bygger seg opp over tid fra asymptomatiske forandringer til ukontrollert aktivitet i det inate immunsystemet (autoinflammasjon) med akutt faserespons og ekstravaskulære manifestasjoner til brutt selv-toleranse og progressiv arterieinflammasjon i regi av det adaptive immunsystemet (Weyand CM, 2023). Den transmurale inflammasjonen ses hyppigst i grener av a. carotis externa, spesielt i a. temporalis superficialis. Også arteria vertebralis angripes hovedsakelig ekstrakranialt, og inflammasjonen strekker seg aldri lenger enn 5 mm. forbi penetrasjonen av dura. Arteria carotis interna affiseres også kun ekstra-duralt, men ikke så hyppig som a. vertebralis. Disse funnene tyder på en sentral rolle for lamina elastica. Totalmengden elastiske fibre reduseres betydelig når for eksempel a. vertebralis gjennomborer dura og lamina elastica externa som ligger mellom adventitia og media, kan ikke lenger gjenfinnes. Man har diskutert soleksposisjon og aldersforandringer er mulige årsaksfaktorer. Ved inflammasjonen øker sekresjonen av IL-12, IL-23, IL-6 og INF-y som tiltrekker makrofager fra benmargen. TNF, PDGF og VEGF produseres. T-cellene aktiverer dendrittiske celler som utskiller kemokiner (CCL 18, 19, 20, 21), IL-6 og IL-18. Også IL- 32 uttrykkes sterkt i arteriene ved AT (Gran JT, 2002). Akutt faserespons skjer i lever og fører til høy CRP og SR. Kjempeceller er multinukleære og av typen klassisk aktiverte makrofager og Langerhans kjempeceller. Selv om en bruker begrepet “kjempecelleartritt” om arteritis temporalis, er disse kjempecellene ikke unike for tilstanden. De kan påvises ved blant annet Takayasus arteritt, granulomatose med polyangiitt (GPA/Wegeners), fremmedlegemer, sarkoidose, infeksjoner og i lungevev ved COVID-19 infeksjon (Tian S, 2020; Bajocci, 2018).
Ekstrakranial storkarsvaskulitt. Patogenese og histopatologi ved uspesifisert ekstrakranial storkarsvaskulitt er ikke godt undersøkt, men antas å være som ved arteritis temporalis (Lensen KDF, 2016). Årsaken til at kraniale arterier ikke angripes er ukjent.
Symptomer

Klassisk arteritis temporalis
Ved klassisk arteritis temporalis er en gradvis eller akutt utvikling av smerter i hodet kombinert med allmenn-symptomer typisk. Symptomene ved klassisk arteritis temporalis forårsakes av vaskulær iskemi, ofte kombinert med tegn på cytokin-mediert inflammasjon. Symptomene kan omfatte hodepine, kjeve-klaudikasjon, transistent synstap, skalpømhet og klaudikasjon i ekstremitetene. Ubehandlet er det økt risiko for permanent synstap og slag. Andre mulige komplikasjoner er aortaaneurisme, disseksjon og ruptur (Prior JA, 2017).
Allmennsymptomer omfatter ny utmattelse, nattesvette, lavgradig feber, nedsatt appetitt og vekttap. Feber observeres i opp til 40% av tilfellene. Symptomet utgjør 15% av tilstander som utredes for med feber av ukjent årsak blant personer >65 år (Smetana GW, 2002; Myklebust G, 1996).
Aortaaneurisme: Forekomsten av aortaaneurisme ved diagnose av biopsiverifisert arteritis temporalis er beregnet til ca. 8% totalt og 10% etter 5 års sykdomsforløp (Koster MJ, 2021). Omtrent 80 % av aneurismene er thorakale og 20 % abdominale. Aneurismeutvikling synes ikke å være korrelert til klinisk sykdomsaktivitet, da manifestasjonene kan oppstå ved medikamentelt godt kontrollert sykdom, selv etter inntrådt remisjon og seponering av kortikosteroider. Årsaken til aneurismene antas å være følger av inflammatoriske skader på media, intima og lamina elastica interna i blodåreveggene under det høye trykket som arterievegger utsettes for. Imidlertid kan også kronisk subklinisk inflammasjon kan være av betydning. I den sammenheng viste en biopsistudie av a. temporalis at 50% hadde inflammatoriske forandringer i a. temporalis etter ett år, til tross for full-dose kortikosteroid-behandling (Malszewski JJ, 2017).
Audiovestibulære manifestasjoner (sjelden): Hørselstap, tinnitus, vertigo, spontan nystagmus, øresmerter ses ved arteritis temporalis, men forventes ikke ved utelukkende ekstrakranial sykdom (Amor-Dorado JC, 2003).
Hals og svelg. Opp til 10% merker irritert, tørt svelg med heshet, tørrhoste eller noe ekspektorat. Up to 10% of patients with GCA experience dry or a productive cough (w or without sputum), sore throat, or hoarseness of voice. Årsaken antas å være iskemi i pharynx (Ameer RA, 2023).
Hjerteinfarkt kan ses hyppigere etter diagnostisert arteritis temporalis eller polymyalgia revmatika, særlig blant menn med hypertensjon (Uddhammar A, 2002; Pujades-Rodrigues M, 2020). Omtrent halvparten skjer innen tre måneder før eller etter debut eller residiv av arteritis temporalis. Årsakene er til dels ruptur av plakk relatert til eksaserbasjon av aterosklerose vaskulopati (type 1). Imidlertid ses også arteritt i koronarkar (type2) uten plakk.
Hodesmertene er nye og lokaliseres temporalt, sjeldnere frontalt, oksipitalt eller er generalisert. Noen opplever nummenhet og smerte i hele skalpen ved arteritis temporalis. Symptomene forventes å gå tilbake innen ca. tre dager på behandling med en høy dose kortikosteroider (prednisolon 60mg/dag eller metylprednisolon/SoluMedrol) (Mollan SP, 2020).
Kjeve-klaudikasjon er smerte som oppstår under tygging og må skilles fra kjeveleddsmerter. Smerter relatert til kjeveområdet skyldes affeksjon av arteriegrener utgående fra a. carotis externa. Foruten klassisk kjeve-klaudikasjon gir dette redusert gapeevne, smerter i a. maxillaris gebetet, sår hals, dysfagi og ubehag ved tale. Symptomene forventes ikke ved utelukkende ekstrakranial sykdom (Lim J, 2024).
Klaudikasjon i ekstremiteter er uvanlig. Affeksjon av store arterier fører sjelden til alvorlige stenoser og okklusjoner, men påvises radiografisk (CT, MR, ultralyd) eller scintigrafisk (PET/CT). Differensialdiagnostisk bør en tenke på Takayasus arteritt, aterosklerose, tromboembolier eller disseksjon. Klinisk iskemi eller nekroser i ekstremiteter er uvanlig, men utelukker ikke diagnosen (Almeida-Morais L, 2016: Watts RA, 1989).
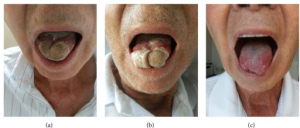
Orale manifestasjoner: Trismus (Kjevesperre), svelgsmerte, dysfagi, hoste og sår hals, heshet, dysartri, nummenhet i kinn, glossitt, makroglossi, leppe og tungenekrose, smerte i tennene, hevelser i hode, nakke og ansikt kan forekomme ved arteritis temporalis. Ved de orale manifestasjoner må vanligere årsaker til sår vurderes differensialdiagnostisk. Disse omfatter karsinom, emboli, rusmidler, resultat av strålebehandling, kjemoterapi, syfilis og tuberkulose (Chehem FCD, 2024).
Perifer artritt forekommer nesten ikke ved arteritis temporalis og omtrent aldri ved diagnose-tidspunkt. Artritt er uvanlig også ved annen storkarsvaskulitt. Imidlertid kan revmatoid artritt, polymyalgia revmatika og arteritis temporalis ha delvis overlappende symptomer ved debut eller oppstå omtrent samtidig/koeksistere (Korkmaz C, 2017).
Polymyalgia revmatika (PMR) forekommer hos ca. 40% og kan debutere før, etter eller samtidig med arteritis temporalis eller uspesifisert ekstrakranial storkarsvaskulitt (Korkmaz C, 2017).
Sentralnervesystemet ved arteritis temporalis: Hyppigheten av apopleksi ved arteritis temporalis er sannsynligvis noe økt (3%) de første 4 uker av sykdomsforløpet. Slag i tidlig sykdomsstadium, men ofte etter påbegynt behandling (første 4 uker), utgår oftest fra arteria vertebralis gebetet, mens senere er arteria carotis-området av større betydning (Gonzalez-Gay, 2009) Det foreligger kasuistiske meddelelser om ataksi, lateralt medulla syndrom, hemianopsi, demens og hørselstap. Ved angrep av a. facialis/lingualis kan døvhet, tinnitus, smakstap, kjeve-klaudikasjon og tungegangren utvikles (Bonnan C, 2023). Insidensen av slag ved temporalis arteritt etter 50 års alder er estimert til 0,76/100.000 (Samson M, 2015).
Skalpnekrose kan utvikles lokalt over den affiserte arterien. Slike pasienter har ofte alvorlig arteritis temporalis, selv om hudlesjonen per se vanligvis heles fullstendig (Gran JT, Irgens K. 2007).
Slag. Vennligst se “Sentralnervesystemet” ovenfor.
Synsforstyrrelser eller blindhet utvikles hos 6-20 % av pasientene med arteritis temporalis. De fleste rammes før behandlingsstart, men synstap kan oppstå også ut i sykdomsforløpet. Den hyppigste årsaken til synstap er anterior iskemisk optikusnevritt på grunn av vaskulitt i de bakre ciliar-arteriene (a. ciliares posteriores). Mer sjeldent er iskemisk retrobulbær nevritt og okklusjon av a. centralis. Synsforstyrrelsene kan opptre som visuelle hallusinasjoner hos ellers psykisk normale personer (Charles-Bonnets syndrom). Ved diplopi foreligger ofte samtidige okulære iskemiske forandringer. Ved synstap på ett øye er det overhengende fare (25-50%) for blindhet på det andre øyet dersom behandling ikke iverksettes. Tidlig diagnose og behandling er viktig for å redusere risiko for blindhet. Samarbeid med øyelege/øyeavdeling kan derfor være essensielt. Sjeldne orbitale manifestasjoner: Øyesmerter, chemose («Rødt øye»), episkleritt, ptose, ødem av øyelokk, exophthalmus (proptose), oftalmoplegi, abducens parese (6. hjernenerve), oculomotorius parese (3. hjernenerve). Okulære manifestasjoner forventes ikke ved uspesifisert ekstrakranial storkarsvaskulitt, men amaurosis fugax og andre synsforstyrrelser som følge av iskemi i arteria vertebralis gebetet forekommer ved begge tilstander (vennligst se sentralnervesystemet ovenfor) (Gonzalez-Gay MA, 2000).
Vaskulitt i ekstremitetene: Ekstrakraniale store arterier angripes hos opp til 100% av pasientene som også har biopsiverifisert vaskulitt i a. temporalis. Ved angiografi påvises 20-67% av disse, ved 18FDG PET/CT 83% og ved biopsi kan vaskulitt ses hos alle (Östberg G, 1973; Gribbons KB, 2020). Særlig affiseres aorta og de nærmeste grenene, inklusive a. carotis, a. subclavia og a. brachialis.
Øyet. Vennligst se synsforstyrrelser ovenfor.
Differensialdiagnoser ved akutt hodepine
Subaraknoidal blødning (nakkestivhet), apopleksi (blødning/infarkt), sinusvene-trombose (utreding: CT med venefase), pseudotumor cerebri (stasepapille), meningitt / encefalitt / sinusitt, tumor cerebri, cerebral abscess arterie-disseksjon.
Ekstrakranial/non-kranial storkarsvaskulitt
Med sensitiv bildediagnostikk har en som i autopsistudier, sett at vaskulitt i aorta og tilgrensende store kar er en manifestasjon ved arteritis temporalis, men også uten at temporalarteriene er affiserte (Bossert M, 2011; Lensen KDF, 2016). Det er imidlertid ikke klarlagt om slik ekstrakranial/non-kranial vaskulitt i store arterier er en egen sykdom eller en undergruppe av arteritis temporalis.
Allmenntilstanden er ved ekstrakranial/non-kranial vaskulitt påvirket i form av utmattelse, redusert appetitt, vekttap, nattesvette, slik som som ved klassisk arteritis temporalis. Polymyalgia revmatika kan ses også ved denne tilstanden og noen utvikler aorta-aneurisme (oftest thorakalt). Symptomene er lite karakteristiske og forsinker ofte diagnosen, selv om blodprøver indikerer inflammasjon. Risikoen for synstap er liten.
Synstap er uvanlig. Pasientene har ikke tinning-smerter eller kjeve-klaudikasjon og øye-symptomer er uvanlig. Få har symptomer direkte relatert til organ-affeksjonen i arteriene (“silent vasculitis”). Alderen er gjennomsnittlig noe lavere ved debut sammenlignet med ved temporalis-biopsi positive (AT) tilfeller. Diagnostisk forsinkelse er større enn ved klassisk arteritis temporalis (Skaug HK, 2023; Lensen KDF, 2016).
Undersøkelser
Anamnesen kartlegger aktuelle symptomer (se ovenfor) hos personer i aktuell aldersgruppe (over 50 år). Spesielt etterspørres generell sykdomsfølelse som nattesvette og vekttap, ny polymyalgi, ny hodepine, lokal ømhet i tinning, nye synsforstyrrelser, klaudikasjon under tygging (kjeve-klaudikasjon), skalpømhet, sår hals og ny heshet, og blodprøver som viser høy CRP og/ eller blodsenkning (SR),
Klinisk undersøkelse. I tillegg til en generell status, er det aktuelt å palpere arteria temporalis som kan fremstå som distinkt øm og fortykket i forløpet ved kranial manifestasjon. Ved symptomer palperes også occipital-arterier og skalpen. Ekstrakranial manifestasjon er klinisk sjelden påvisbar, men en bør palpere perifer puls ved håndledd (a. radialis), på føttene (a. dorsalis pedis eller a tibialis posterior) og på halsen (a. carotis), fordi stenoser og tegn på redusert blodsirkulasjon forekommer i enkelte tilfeller og tilstanden bør avgrenses fra Takayasus arteritt som typisk forårsaker stenoser og okklusjoner. Ved auskultasjon undersøkes systematisk for stenoselyder fra arteriestenoser over precordiet, hals, lysker og abdomen. Blodtrykk måles på begge overarmer (asymmetrisk affeksjon i subclavia/ brachialis-arterier).
Laboratorieprøver. Rutineundersøkelse omfatter CRP som viktigste serologiske indikator på inflammasjon. Senkningsreaksjon (SR) er også en god parameter. Supplerende prøver kan omfatte Hb, leukocytter med differensialtellinger, elektrolytter, lever-, nyre- og thyreoidea-funksjonsprøver, kreatin kinase (CK), glukose, HbA1c og urin-stiks. Differensialdiagnostisk kan antistoff som anti-CCP, ANA og ANCA være aktuelt. -En forventer høye inflammasjonsparametere, hvorav CRP er mer spesifikk enn SR. Ved ubehandlet arteritis temporalis er både SR og CRP forhøyet hos over 95%. Tresifrede verdier er ikke uvanlig, særlig hvis sykdommen har vært udiagnostisert og ubehandlet over tid. I alt er det funnet at 90% av pasientene har SR >50mm/t, 10% har SR < 50mm/t og 3,6% har SR under 30 mm/t (Kermani TA, 2012). Initialt kan ca. 10% ha normal CRP eller SR, men de fleste utvikler deretter forhøyede verdier. Normale verdier for både SR og CRP sees hos kun 4% av pasientene (Kermani TA, 2012). Hvis normal CRP, men høy SR bør en differensialdiagnostisk vurdere paraproteinemi med høy IgG eller IgM eller annen blodsykdom. Det finnes ingen spesifikke tester for arteritis temporalis eller andre typer storkarsvaskulitt. Leukocytose sees hos omkring 1/3 (og etter påbegynt steroid-behandling). Trombocytose hos 1/3. Tilsvarende forventes ved utelukkende ekstrakranial manifestasjon. Laboratorieprøver for differensialdiagnostikk kan omfatte: Leukocytter med differensialtellinger, trombocytter, blodutstryk (leukemi), CK (polymyositt/dermatomyositt), TSH, thyreoidea-antistoffer (hypotyreose/thyreoiditt) og serumelektroforese.
-Immunologiske undersøkelser. Det forventes ikke utslag i immunologiske tester. ANCA kan være aktuell for å utelukke ANCA-vaskulitt som differensialdiagnose.
Øyelege. Ved synsforstyrrelser suppleres med snarlig øyelege-undersøkelse. Fundoskopi kan initialt avdekke avblekning og ødem på synsnervepapillen, eventuelt også atrofi. Supplerende bildediagnostikk kan bidra til å sikre diagnosen (se nedenfor) (Heron E, 2022).
Bildediagnostikk
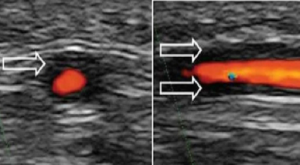
–Ultralyddiagnostikk (UL) anbefales som førstelinje bildediagnostikk. Temporalis arteriene undersøkes initialt, helst suppleres med ultralyd av axillaris-arterier (Bosch P, 2023; Dejaco C, 2023), også fordi 40% av pasientene ikke har a. temporalis-manifestasjoner (ekstra-kranial /non-kranial vaskulitt). Undersøkelsen tar 15-20 minutter. Moderne utstyr gir en oppløsning på 0,1 mm. i områder innen 1 cm fra hudens overflate. A. temporalis communis undersøkes sammen med arteriens frontale og parietale grener. Disse vurderes i både longitudinal og transvers plan på begge sider av hodet. Arteria axillaris lar seg undersøke fra aksillene. Sensitivitet og spesifisitet er estimert til hhv 77% og 96% for ultralyd av a. temporalis sammenlignet med klinisk diagnose (Schmidt WA, 2018). Ultralyd gjør at en kan undersøke hele temporalis-arterienes lengde uten invasiv diagnostikk ved arteritis temporalis. Også axillaris-arteriene er aktuell å undersøke. Ultralydapparater er tilgjengelige på alle revmatologiske og radiologiske avdelinger og brukes regelmessig i diagnostikken. Dersom en bilateralt finner typiske arteritt-tegn er spesifisiteten nær 100%, men undersøkelsen har lav sensitivitet (43% i en metaanalyse (Arida A, 2010), slik at en del tilfeller kan overses. Særlig kan små forandringer i vasa vasorum i tidlig sykdomsfase overses (Restuccia G, 2012). Bruk av UL av arteria temporalis kan uansett bedre treffsikkerheten ved biopsi. Særlig vil funn av ødem rundt arterien («halo») lokalisere områder med aktiv inflammasjon. Forugående kortikosteroid-behandling reduserer imildertid undersøkelsens sensitivitet (Pinnell J, 2023), og haloen forsvinner som regel etter 2-3 ukers steroidbehandling (Gran JT. 2005) og . Ved ekstrakranial manifestasjon kan vaskulitt-tegn vises i store arterier som a. axillaris, carotis og vertebralis. Sist nevnte er av størst betydning når det gjelder risiko for slag relatert til sykdommen. Det er utviklet et OMERACT skåringssystem for vurdering av temporalis arteritt (Dejaco C, 2022). Vennligst se også eget kapittel om ultralyd-undersøkelser ved vaskulitt.
–Computertomografi (CT) av aorta kan gjøres som del av utredningen for å utelukke tidlige tegn til aneurisme eller disseksjon. En vil da også ha et utgangspunkt for senere kontroll-undersøkelser. Ikke sjelden er fortykket karvegg i aorta og tilgrensende kar på CT inngangsporten til storkarsvaskulitt diagnosen. Veggfortykkelse over 2,2mm kan indikere vaskulitt (Berthod PE, 2018). For å utelukke aneurismeutvikling i forløpet og etter seponering av behandling er det aktuelt å gjøre CT aorta eller ekkokardiografi og CT abdomen. Undersøkelsene kan gjentas hvert annet år i 6 år eller lenger. Dette gjelder både ved klassisk arteritis temporalis og ekstrakranial storkarsvaskulitt. Arteriestenoser og okklusjon i store kar forekommer, men er sjelden og ikke så vanlig som ved Takayasus arteritt.
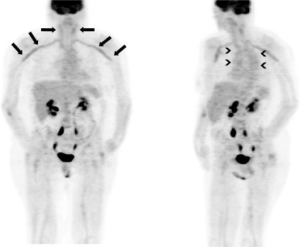
-PET/CT brukes i økende grad for å kartlegge sykdomsutbredelsen (Dejaco C, 2023). Undersøkelsen kan påvise utbredelse av aktiv vaskulitt i store- og mellomstore arterier, fortrinnsvis før behandling med kortikosteroider er påbegynt eller at prednisolon dosen er under 10-15mg/dag. Tidligere autopsistudier (Östberg G, 1973) og nyere bruk av PET/CT har vist høy forekomst utbredt arteritt i store arterier ved temporalis arteritt. Særlig affiseres aorta og de nærmeste grenene, inklusive arterier i ekstremitetene. En tidlig PET/CT studie viste at 74% hadde arteritt i subclavia arterier og 51% i thorakal aorta. Med nyere og mer sensitiv teknologi er en enda større andel (83%) med vaskulitt i store, ekstrakraniale kar påvist. Kontroll av PET/CT funn senere i behandlingsforløpet er mindre nyttig og anbefales sjelden (Blockmans D, 2006). PET/CT egner seg således godt til diagnostikk av ekstrakraniale vaskulitt-manifestasjoner. Med god teknikk fremstilles også arteria temporalis (Nienhuis PH, 2020). Opptak i a. femoralis er ikke uvanlig, men skyldes ofte samtidig forekomst av aterosklerose og ikke nødvendigvis vaskulitt. Bruk av PET/CT begrenses av tilgjengelighet og kostnader (Dejaco C, 2023).
Fluorescin angiografi, indocyanin angiografi, OCTA. De mest aktuelle metodene for å diagnostisere iskemi i øyet utenfor papillo-macula-områdene er intravenøs fluorescein angiografi, indocyanin angiografi eller optical coherence tomography angiography (OCTA) (Casella AMB, 2022).
Biopsi
Biopsi av arteria temporalis sikrer diagnosen og bør tilstrebes. Unntak er der diagnosen er sikker på bakgrunn av typisk anamnese, klinisk undersøkelse og bildediagnostikk ultralyd, gjort av en erfaren undersøker eller PET/CT eller MR utført med optimal teknikk (Dejaco C, 2023). Til tross for behandling med kortikosteroider over et par uke, forventes aktuelle histologiske funn. Generelt har bare 5-10% har negativ histologi. Selv om ultralyd av temporalis-arteriene kan gi sterk mistanke om temporalis arteritt, gjøres vanligvis også biopsi for å sikre diagnosen. Dette fordi sensitiviteten (sikre diagnosen) er lav ved ultralyd alene (Arida A, 2010). Ved negativt funn og klar mistanke kan man be om ytterligere snitt av det allerede biopserte karet. Viser de nye snittene også normale funn og mistanken om arteritis temporalis fremdeles er til stede, har det vært vanlig å anbefale ny biopsi fra motsatt side. Imidlertid er sjansen for å påvise patologiske forandringer ved ny biopsi etter en forutgående negativ biopsi liten (<10%). Ideelt bør biopsien ha en lengde på tre centimeter. Dette fordi sykdommen har en segmental og ikke kontinuerlig utbredelse. I praksis er korte biopsier vanlig. En bør da være klar over at biopsi med lengde < 1cm, ikke med tilstrekkelig sikkerhet kan utelukke diagnosen. Ved fravær av symptomer, men påvist ekstra-kranial manifestasjon er biopsi positiv hoc ca. 50% (Amer MA, 2021). Ekstrakranial manifestasjon egner seg ikke for utredning med biopsi, utenom ved operative prosedyrer på annen indikasjon (aneurisme, disseksjon). -Kortikosteroider. Allerede igangsatt behandling med kortikosteroider reduserer ikke nevneverdig sjansen for å påvise patologiske forandringer ved behandling over kort tid. Etter under to uker fra behandlingsstart gjenfinnes vaskulitt hos 78%, etter 2-4 uker hos 65% og etter mer enn 4 uker hos 40% (Narvaez J, 2007). -Histologi. Typiske biopsi-funn ved temporalis-biopsi er en blandet infiltrasjon i karveggen av mange typer inflammatoriske celler slik som epiteloide celler, lymfocytter, neutrofile, eosinofile og fibroblaster. Ofte er også lamina elastica interna skadet. Kjempeceller ses hos ca. 50% (Stacy RC, 2011). Med sikkert patologisk funn ved arteritis temporalis kreves transmural infiltrasjon av betennelsesceller og kjempeceller. Med sannsynlig patologisk funn kreves minimum transmural inflammasjon. Inflammasjon i a. temporalis er ikke helt spesifikk for arteritis temporalis og er også beskrevet ved polyarteritis nodosa (PAN), granulomatose med polyangiitt (GPA, Wegeners granulomatose) (Haugeberg G. 1998) og Kimuras sykdom (Bajocci, 2018).
Ekstrakranial arteritis temporalis diagnostiseres på bakgrunn av systemisk inflammasjon og bildediagnostikk (ultralyd, PET/CT, MR, CT). Biopsi er sjelden aktuelt. Uspesifikke symptomer medfører ofte lang latenstid før diagnosen er sikker, noe som særlig gjelder ved uspesifisert ekstrakranial storkarsvaskulitt. En studie fant at latenstid fra symptomdebut til diagnose var 9 uker for arteritis temporalis mens den var nesten det dobbelte for uspesifisert ekstrakranial sykdomsmanifestasjon (Prior JA, 2007).
Juvenil arteritis temporalis medfører fortykket temporalis arterie, men har vanligvis et annet histologisk bilde med panarteritt, eosinofile infiltrater og fravær av granulomer og kjempeceller (Lie JT, 1975).
Screening for kreft. Generelt anbefales ingen cancer screening, da det ikke foreligger noen sikker økt hyppighet av maligne lidelser verken ved arteritis temporalis eller PMR (Myklebust G, 2002). Imidlertid rammer begge tilstander eldre personer der forekomsten av kreft er relativt høy. Det kreves derfor nøye klinisk undersøkelse av disse pasientene. Maligne sykdommer kan dessuten debutere med muskelsymptomer. Risiko ved uspesifisert ekstrakranial storkarsvaskulitt er ikke godt undersøkt.
Kriterier for diagnose
Kriterier for arteritis temporalis er først og fremst konstruert for vitenskapelig bruk (klassifikasjonskriterier). I klinisk praksis er de veiledende. Klassifikasjonskriteriene egner seg ikke for en tidlig diagnose, da de ikke tar hensyn til at sykdomsbildet utvikles gradvis. Det er verdt å merke seg at ACR-kriteriene ikke krever positiv biopsi eller bildediagnostikk. Allikevel anbefales biopsi i diagnostisk øyemed, alternativt bildediagnostikk, oftest ultralyd-undersøkelse av en erfaren spesialist på området. En modifisert utgave av ACR 1990 kriteriene som kan brukes i klinisk praksis er beskrevet nedenfor:
Diagnostiske kriterier for AT (modifisert av JTG etter Hunder GG, ACR 1990): tre eller flere av følgende:
- Alder 50år eller eldre
- Nyoppstått hodepine
- Arteriebiopsi som viser transmural inflammasjon
- Lokal ømhet eller pulsreduksjon av en av hodets overfladiske arterier
- Forhøyet SR (og/eller CRP)
- Eksklusjon av andre sykdommer
| ACR/EULAR klassifikasjonskriterier (2022): Disse baseres på vekting og av poeng-score og vil kreve alder ≥ 50 år og påvist vaskulitt ved bildediagnostikk i tillegg til kliniske kjenneteg (Ponte C, 2023). | |||
| Kliniske symptomer | pkt | Undersøkelser | pkt |
| Morgenstivhet i skuldre/nakke | +2 | Senkningsreaksjon (SR) ≥ 50 mm./t, CRP ≥ 10 mg/L | 3+ |
| Plutselig synstap | +3 | a. Temporalis-biopsi positiv eller ultralyd med halo | +5 |
| kjeve eller tunge-klaudikasjon | +2 | a. Axillaris: Bilateral affeksjon | +2 |
| Smertefull hodebunn | +2 | FDG-PET med tegn til inflammatorisk aktivitet i hele aorta | +2 |
| Palpasjon av a. temporalis med patologisk funn | +2 | ||
| Klassifikasjon når ≥ 6 punkter foreligger. Sens. 87%, spes. 95% | |||
Spesielle sykdomsgrupper
AT med normal SR / CRP: Dette er en sjelden problemstilling, men er rapportert hos opp til 4% av tilfellene (Kermani TA, 2012). Diagnosen AT skal her stilles histologisk, og bør komme etter meget nøye vurdering. Enkelte har hevdet at behandlingsrespons kan sees ved at SR/CRP avtar innen normalområdet.
AT hos personer under 50 års alder: Både klassisk temporalis arteritt og ekstrakranial storkarsvaskulitt er ytterst sjeldne i denne aldersgruppen. Andre årsaker til symptomer er mer sannsynlig, slik at spesielt nøye differensialdiagnostisk utredning kreves. Annen systemisk vaskulitt, særlig Takayasus arteritt eller ANCA-vaskulitt, Kimura sykdom er blant differensialdiagnosene (Akalin T, 2014). De fleste vil, uansett diagnose, initialt føle noe lindring av høye doser kortikosteroider, men får symptomresidiv tidligere enn forventet under dosenedtrapping.
AT hos personer med asiatisk eller afrikansk genetisk bakgrunn: Tilstandene er mye sjeldnere enn blant kaukasiere. Differensialdiagnostiske overveielser er desto viktigere (Watts RA, 2022).
Juvenil arteritis temporalis
Definisjon. Juvenil arteritis temporalis er ikke samme sykdom som AT. Tilstanden ble første gang beskrevet i 1975 (Lie JT, 1975). Alle aldersgrupper kan angripes, inklusiv barn. De fleste er unge, under 40 år
Symptomer og kliniske funn. Typisk symptom er palpabel, knutete, fortykket temporalis arterie i en tinning, sjelden bilateralt. Vanligvis er lesjonen smertefri og allmenntilstanden er ikke påvirket.
Laboratorieprøver viser normale eller nær normale CRP og SR, men noen tilfeller med eosinofili er beskrevet.
Biopsi med histopatologisk uttalt inflammasjon med lymfocytter, eosinofile, plasmaceller og endotel-proliferasjon er karakteristisk. Også intima-proliferasjon og skadet media forventes.
Differensialdiagnoser omfatter Kimuras sykdom som kan ha et lignende histologisk bilde. Imidlertid angriper Kimuras sykdom oftest etniske asiater og medfører typiske subkutane, store lesjoner (>2 cm) med andre lokalisasjoner, samt hovne spyttkjertler.
Behandling med prednisolon (initialt 0,5mg/kg) med rask nedtrapping og seponering over et par måneder er gitt (Pipinos II, 2006). Det er mulig behandlingen medvirker at sykdommen går raskt tilbake. Residiv, synstap, aneurismer eller alvorlige komplikasjoner er uansett ikke å forvente
Litteratur: Lie JT, 1975; Kolman OK, 2009; Bollinger A, 1986
Differensialdiagnoser
Hodepine av annen årsak (vanligvis ikke høy senkningsreaksjon (SR) og CRP, lavere aldersgrupper)
- Aneurisme i a. temporalis (idiopatisk)
- Borrelia infeksjon
- Tempo-mandibulær smerte
- Cluster-hodepine (Hortons hodepine)
- Episoder (cluster) med ekstrem hodepine
- Fibromyalgi
- Kronisk, oftest kvinner, normale blodprøver
- Glaukom
- Uklart syn, farger i synsfeltet
- Hjerneblødning
- Svært akutt
- Hjernesvulst
- Andre symptomer: kramper, pareser, redusert sensibilitet, kvalme
- Hypertoni
- Hypertensiv krise
- Juvenil arteritis temporalis er ikke samme sykdom som AT (se under spesielle sykdomsgrupper ovenfor)
- Migrene
- Anfallsvis, lysskyhet, kvalme
- ANCA-vaskulitt (GPA, MPA, EGPA) og PAN
- Infeksjoner
- Tuberkulose, abscesser
- Malignitet
- Polymyalgia Revmatika (PMR)
- PRES (Posterior reversibel encefalopati syndrom)
- Hjerneødem og synstap, blant annet ved SLE
- Spenningshodepine
- Smertefulle nakkemuskler
- Trigeminusnevralgi
- “Strømstøt”, hake eller kinn
Ekstrakraniale manifestasjoner
- ANCA-vaskulitt
- Aterosklerose
- Autoimmun sykdom av annen årsak
- Behcets sykdom
- Cogans syndrom
- IgG4 relatert aortitt
- Infeksjoner
- HIV, Syfilis, tuberkulose, hepatitt
- Polyarteritis nodosa
- Relapsing polykondritt
- Revmatoid artritt
- Sarkoidose
- Systemisk lupus (SLE)
- VEXAS syndrom.
Skåring av sykdomsaktivitet
Det foreligger ikke gode systemer for å skåre sykdomsaktivitet ved arteritis temporalis eller ekstrakranial storkarsvaskulitt. Blodprøver som indikerer inflammasjon, spesielt CRP, forventes å være innen referanseområdene når behandlingen er tilstrekkelig. Blodsenkningsreaksjon (SR) er mindre spesifikk og kan være forhøyet av andre årsaker, inklusiv hyper-gammaglobulinemi (høy IgG).
EULAR definerer sykdomsaktivitet basert på pågående typiske symptomer (se ovenfor) og minst ett av følgende: sykdomsaktivitet ved bildediagnostikk eller biopsi, iskemiske komplikasjoner eller vedvarende forhøyede inflammasjonsmarkører (Hellmich B, 2020).
Verken BVAS-kriterier utviklet for ANCA-vaskulitt eller NHI/Kerr kriterier (Kerr GS, 1994) som ble utviklet for Takayasus arteritt er dessverre lite anvendelige ved arteritis temporalis (Karmani TA, 2016; Magani L, 2011).
Naturlig sykdomsforløp
Ubehandlet vil symptomer vedvare og risiko for komplikasjoner øker fortløpende. Ved arteritis temporalis er en spesielt bekymret for blindhet. Både arteritis temporalis og uspesifikk ekstrakranial storkarsvaskulitt kan utvikle aortaaneurismer. Behandlingsrefraktære tilfeller blant menn vurderes med tanke på VEXAS syndrom.
Behandling
Målet med behandlingen er å fjerne symptomer og å hindre sykdoms-komplikasjoner, inklusive synstap. Ved sterk mistanke om arteritis temporalis kan en kan starte behandling før svar på biopsi eller bildediagnostikk foreligger. Dette for å redusere risiko for irreversibelt synstap. Ellers er behandlingsopplegget likt mellom arteritis temporalis og ekstrakranial sykdom. Behandlingsresponsen på kortikosteroider er god, men det er betydelige individuelle variasjoner. Det finnes derfor en rekke ulike doserings-regimer (Dejaco C, 2023).
Nåværende medikamentell behandling baseres hovedsakelig på glukokortikoider, men også tocilizumab og metotreksat i noen tilfeller.
Det er vist at glukokortikoider virker hemmende på proinflammatoriske interleukiner IL-6 og IL-17 som er sentrale mediatorer ved vaskulitt (Hill CL, 2017). Nesten alle har hatt høy CRP før behandlingsstart, og denne er en god parameter for sykdomsaktivitet i tillegg til klinisk vurdering. CRP bør i behandlingsforløpet bli nær normal og holdes der. Det anbefales å anvende prednisolon fremfor prednison fordi prednison må hydroksyleres i lever til prednisolon som er den aktive substansen. Det er ikke foretatt studier som har evaluert dosering i forhold til pasientens kroppsvekt. Seponeringsforsøk etter 2 år er aktuelt, tidligere i enkelte tilfeller.
Ved ukomplisert arteritis temporalis (fravær av synsforstyrrelser, trismus, nevrologiske manifestasjoner eller skalpnekrose) er startdosen oftest 40 mg/dag (for eksempel 30mg morgen + 10 mg ettermiddag). Dose-reduksjon er individuell og persontilpasset og det finnes flere forslag til regimer. En kan i utgangspunktet redusere dagsdosen med 5 mg hver- til hver tredje uke til dagsdosen er 15-20 mg innen 1-3 måneder. Deretter reduseres langsommere med et mål om at dosen er 5-10 mg/dag eller lavere innen ett år fra behandlingsstart (Hellmich B, 2020). Man kan for eksempel redusere dagsdosen med 1,25 mg ukentlig i 4 uker eller med 2,5 mg hver 3. uke til dosen er 10mg/dag. Hvis tilfredsstillende forløp, kan en deretter å forsøke videre reduksjon med 1,25 mg hver tredje uke til dosen er 5mg/dag.
Behandling av komplisert arteritis temporalis: Startdose med kortikosteroider ved synsforstyrrelser: Kontrollerte studier foreligger ikke, men 60 mg prednisolon daglig anses som en effektiv startdose (Dasgupta B, 2010). Først starter en ofte med 250-1000mg metylprednisolon (SoluMedrol) i.v. daglig i 3 dager. Deretter prednisolon. Dosen reduseres gradvis over flere uker, tilsvarende som ved ukomplisert sykdom (se ovenfor). Dosereduksjonen må skje under nøye overvåkning av sykdomsutviklingen hos den enkelte. Vedlikeholdsdose prednisolon 2,5 -10 mg opprettholdes i ofte i minst ett år. Med vedlikeholdsdose forstås den daglige dosen av peroralt kortikosteroid som i rimelig grad kontrollerer sykdomsmanifestasjonene (og CRP) og som ansees a kunne beskytte mot sykdomskomplikasjoner. Biopsi og PET/CT undersøkelser tyder på at en viss grad av vaskulitt består, selv om CRP og andre tilgjengelige biomarkører for inflammasjon er normalisert. Det gjenstår å se om dette bør ha behandlingsmessige konsekvenser.
Acetylsalisylsyre (ASA). Her foreligger usikkerhet for nytte/risiko ratio. EULAR anbefaler ikke rutinemessig bruk av platehemmere eller antikoagulasjon ved storkars-vaskulitt (Hellmich B, 2020), mens andre eksperter gjør det (Gonzales-Gay MA, 2019). Dersom individuell vurdering tilsier risiko for iskemisk cerebrovaskulær eller kardial hendelse, kan tillegg av acetylsalicylsyre 75 mg/d gis forutsatt fravær av kontraindikasjon.
Syrepumpe-hemmer (for eksempel pantoprazol 20-40 mg) bør vurderes som forebyggende mot ulcus ventriculi. Pasienter med symptomgivende ulcus ventriculi siste 6 måneder skal profylaktisk behandles med protonpumpe-hemmer eller misoprostol. Vær oppmerksom på at syrepumpe-hemmere kan redusere opptak av kalsium og øke risiko for osteoporose.
Kalsium og D-vitamin substitusjon. Kvinner skal under kortikosteroid-behandling få tilbud om profylaktisk kalsium og D-vitamin (Calcigran Forte og andre), eventuelt også osteoporose-behandling med østrogener eller bisfosfonater for å motvirke osteoporose.
csDMARDs. Sykdommens etiologi og patogenese er ikke er helt forstått. Det kan foreligge individuelle ulikheter innen samme diagnose. Slike forskjeller kan forklare ulik respons på standard behandling, og at noen har effekt av enkelte supplerende medikamenter, mens de er uvirksomme hos andre. Pasienter med behov av høye vedlikeholdsdose som prednisolon > 10 mg daglig bør vurderes for tilleggsbehandling. Metotreksat er førstevalg blant DMARDs, selv om studier viser liten eller usikker effekt på gruppenivå (Yates M, 2014).
Biologisk behandling med tocilizumab (RoActemra) (IL-6R antagonist) har i placebokontrollerte studier vist å kunne redusere behovet for kortikosteroider og gi færre sykdomsresidiv (Stone, JH NEJM, 2017). EULAR anbefaler tocilizumab i selekterte, behandlingsrefraktære tilfeller som et alternativ til metotreksat (se ovenfor) (Hellmich B, 2020). I Norge er tocilizumab godkjent til behandling av temporalis arteritt hos voksne som ikke tåler eller ikke har tilstrekkelig effekt av prednisolon og tillegg av metotreksat (nyemetoder.no). Anbefalt dose er 162 mg/uke s.c. En bekymring er at en tredel av pasientene under tocilizumab fortsatt har tegn på vaskulær inflammasjon ved MR angiografi, til tross for klinisk remisjon (Reichenbach S, 2018). I tillegg kan sykdomsprogresjon ses til tross for normal CRP, delvis også lav SR under tocilizumab. Ulemper er også økt infeksjonsrisiko og at medikamentet er kostbart. En Cochrane gjennomgang av tilgjengelige data anbefaler uansett mer forskning for bedre å avklare effekt og mulige bivirkninger over tid (Antonio AA, 2022).
IL-12 og IL-23 er inflammasjons-mediatorer ved arteritis temporalis. En åpen studie med 25 pasienter har vist lovende resultater (Conway R, 2018), men utprøving i større, kontrollerte studier er nødvendig før en kan konkludere om medikamentet er nyttig ved AT.
T-celle hemmeren abatacept er testet i en placebokontrollert, randomisert studie der behandlingen resulterte i færre tilbakefall enn placebo (52% vs. 69%) og varigheten av remisjonene var lengre i behandlingsgruppen (10 mnd. versus 4 mnd.) (Langford CA, 2017). Også for abatacept gjenstår å se om behandlingen er nyttig når nærmere utprøving er gjennomført.
TNF-alfa-blokkere har i studier av arteritis temporalis til forskjell fra Takayasus arteritt ikke bekreftet behandlingsgevinst (Samson M, 2018).
Andre: JAK/STAT hemmere, PD-1 agonister og MMP-9 blokkerende substanser er under utprøving i studier (Schäfer VS, 2023).
Komplikasjoner under behandling
Aortaaneurisme. Årsaken til aortaaneurisme er sannsynligvis en kombinasjon av svekket aortavegg på grunn av inflammasjon og det høye trykket som befinner seg i arterier. Vennligst se også avsnittet “Symptomer” ovenfor i dette kapitlet.
Apopleksi/CNS behandles i samarbeid med nevrologisk avdeling. Cerebrovaskulære katastrofer sees sannsynligvis ikke hos flere enn 3-5 %. Vennligst se under avsnittet “Symptomer” ovenfor.
Artritt: Perifer arteritt kan behandles med intra-artikulære injeksjoner av triamcinolon (Lederspan). Ved polyartritt bør utvikling av revmatoid artritt som differensialdiagnose vurderes. Ved behandlingstrengende oligoartritt kan DMARDs i form av metotreksat forsøkes. Se også i avsnittet “Symptomer” ovenfor.
Diabetes mellitus: Alle som får kortikosteroider bør sjekkes for utvikling av diabetes innen 1-2 uker (Fastende blodsukker, urin stiks, HbA1c).
Divertikulose. Pasienter med symptomgivende divertikulose skal spesielt informeres om faren for gastrointestinale komplikasjoner (perforasjon). Høye doser kortikosteroider kan disponere for perforasjon. Tocilizumab kan være kontraindisert.
Kortikosteroider uten effekt: Dette er svært sjelden, og diagnosen bør i første omgang revurderes. Hos noen pasienter kan man oppleve manglende respons på prednisolon, mens metylprednisolon derimot av uforklarlige grunner gir ønsket effekt. Årsaken kan da være genetisk betinget resistens mot glukokortikoider (Smutny T, 2019). En annen sjelden årsak er redusert gastrointestinale absorpsjon, slik at parenteral administrasjon av tilsvarende doser gir bedre effekt.
Osteoporose: Kortikosteroid-behandling øker risiko for osteoporose, særlig blant kvinner; profylaktisk kalsium og D-vitamin (Calcigran Forte), eventuelt også østrogener eller bisfosfonater. Måling av bentetthet/benmasse (DXA-scanning) tidlig i behandlingsforløpet anbefales.
Persisterende høy SR/CRP til tross for klinisk behandlingseffekt: Det foreligger ingen dokumentasjon på hva en manglende biokjemisk respons på behandlingen skyldes. Tidligere ble det antatt at slike pasienter ofte hadde koeksisterende malign lidelse. Aktiv inflammasjon i store kar er også en mulighet. Indikasjon for videre utredning med PET/CT vurderes i hvert enkelt tilfelle.
Tuberkulose Pasienter med tidligere aktiv tbc. sjekkes med IGRA-test og henvises lungelege dersom positivt funn. ‘
Stenoser eller okklusjon i store arterier forekommer, men er ikke så vanlig som ved Takayasus arteritt. Samtidig aterosklerose bør vurderes.
Synstap kan utvikle seg i sykdomsforløpet: Vennligst se i avsnittet “Symptomer” ovenfor.
Retningslinjer / anbefalinger
- ACR/EULAR 2022 klassifikasjonskriterier, Ponte C, 2023
- Dejaco C, 2023. Behandling “treat to target”
- EULAR bildediagnostikk 2023 (Dejaco C, 2023)
- OMERACT sonografi-score (Dejaco C, 2022)
- EULAR 2018 update. Hellmich B, 2019
- EULAR 2018: Monti S, 2019
- British Guidelines 2020 Mackie SLE, 2020
- Norsk Revmatologisk Forening/Legeforeningen
Oppfølging
Diagnosen temporalis arteritt og annen vaskulitt i store kar bør vurderes initialt av revmatologisk poliklinikk, avdeling eller hos praktiserende spesialist. Oppfølging etter start av behandling gjøres initialt vanligvis hos spesialist, men erfarne allmennleger kan også utføre oppfølgingen.
Monitorering gjøres på bakgrunn av symptomer, kliniske funn og CRP (eller SR). Hyppigheten av kontroller baseres på det individuelle forløpet og kan på sikt være hver tredje-sjette måned over 1-2 år. Månedlige kontroller av CRP til sykdommen er i remisjon med fravær av aktuelle symptomer og normalisering av CRP, er aktuelt (Dejaco C, 2023). En kan i tillegg vurdere toleranse for behandlingen, deriblant utelukke steroid-utløst diabetes. Kontrollene kan delvis gjøres hos allmennlege/fastlege. Kontrollintervallene hos revmatolog kan forlenges dersom kommunikasjonen med pasientene og forløpet tillater det. På lengre sikt er oppfølging for å utelukke aorta-aneurisme (se nedenfor):
Blodsukker bør måles initialt og i begynnelsen av behandlingsforløpet (steroid-utløst diabetes).
Bentetthetsmåling (osteoporose) innen ca. tre måneder er aktuelt.
Månedlige kontroller av CRP til sykdommen er i remisjon med fravær av aktuelle symptomer og normalisering av CRP, samt under reduksjon av prednisolon er aktuelt.
Aorta-aneurisme-utvikling kan utelukkes med CT aorta (ikke nødvendigvis med kontrastmiddel) eller ekkokardiografi og CT abdomen som utføres for eksempel hvert annet år i 6-7 år.
Residiv. De vanligste symptomer på tilbakefall er lokalisert hodepine og muskelsmerter (polymyalgia revmatika). I blodprøver vil CRP og senkningsreaksjonen (SR) øke hos ca. 80% ved tilbakefall. Ved et lite alvorlig tilbakefall økes dosen til den som sist fungere bra. Vanligvis kan Prednisolon etter noen uker igjen reduseres gradvis og avsluttes etter 1-3 års behandling. Dersom et tilbakefall omfatter alvorlige komplikasjoner som synstap, velges ofte re-behandling som ved sykdomsdebut.
Prognose
Tilbakefall/residiv. Forløpet er individuelt. Gjennomsnittlig får omtrent en av tre (34%) tilbakefall av sykdommen i løpet av Prednisolon-reduksjonen, de fleste (25%) det første året (Keramni TA, 2015). Dersom PMR og arteritis temporalis eller ekstrakranial storkarsvaskulitt opptrer samtidig, kan sykdommen ha et mer langtrukkent og alvorlig sykdoms forløp enn pasienter med AT alene. Behovet for langvarig behandling øker (Lensen KDF, 2016).
Behandlingsvarighet og seponering: En prospektiv studie viste at de fleste pasientene fikk minst en varig skade av sykdommen, men oftere av behandlingen. Komplikasjoner fra store arterier (29%) og øyne (22%) var vanligst. Bivirkninger av kortikosteroider omfattet katarakt, osteoporose og vektøkning (Karmani TA, 2018). Ved arteritis temporalis også ved ekstrakranial manifestasjon prøves seponering etter langsom medikament-reduksjon, generelt etter ca. 2 år.
Eksaserbasjon etter seponering: Binyrebarken kan bruke opptil 2 år på å opparbeide full funksjon etter langvarig suppresjon gjennom kortikosteroid-behandling. Dette kan være en av grunnene til at pasienter etter seponering klager over symptomer som ikke kan relateres til sykdomsresidiv, men isteden representerer en form for biokjemisk abstinens (sekundært Addisons syndrom). Utredning hos voksne omfatter gradvis reduksjon av dosen til prednisolon 5mg/dag eller lavere. Etter to måneder på lav dose måles serum-kortisol minst 24 timer etter siste prednisolon-inntak. Morgen-kortisol-verdier under referanseområdet tyder på kortisolmangel. Stigende CRP etter seponering tyder imidlertid på eksaserbasjon.
Mortalitet: Det er per i dag usikkert om pasienter med AT har økt mortalitet sammenlignet med normalpopulasjonen. I en studie fra Danmark var mortaliteten lett økt sammenlignet med befolkningen ellers i samme alder (Baslund B, 2014), mens det er ikke funnet noen forskjell i et norsk materiale (Brekke KL, 2019). Selv om det ikke er statistisk målbart, er det imidlertid klart at enkelte dør av aneurismeblødning (Garen T, 2019).
Litteratur
Ponte C, 2023 (klassifikasjonskriterier)
Cid MC, 2020 (Behandling)
Lensen KDF, 2016 (ekstrakranial storkarsvaskulitt)
Skaug HK, 2023 (norske data)
