BINDEVEVSSYKDOMMER (REV 021-033)
54 Antisyntetase syndrom (ASS) (REV 021, REV 029)
Jan Tore Gran and Øyvind Palm
Kjennetegn på antisyntetase syndrom
Diagnosekoder ICD-10: M35.8 + J99.1 Prosedyrekoder: 6-minutter gangtest: FYFX05. Kapillærmikroskopi: PKFT00. Intravenøs infusjon: WBGM00. Infusjon med gammaglobulin: RPGM05. EKG: FPFE15 ATC koder (for legemiddelstatistikk): L04A A Immunsuppressive legemidler. Behandling med rituksimab: L01XC02. Behandling med cyklofosfamid: L01AA01.
Definisjon
Antisyntetase syndromet (ASS) er en undergruppe av myositt/inflammatorisk myopati som manifesterer seg spesielt med interstitiell lungesykdom, men også myositt og artritt. Initialt kan også feber og kutane manifestasjoner ses. Lungemanifestasjonene varier fra lette til alvorlige og kan progrediere. Navnet henspiller på en gruppe intracellulære enzymer som er essensielle i syntesen av proteiner. Antistoff i blod er høy-spesifikke og inkluderer vanligst anti-Jo-1, noe sjeldnere anti-PL- 7 eller PL-12. Andre spesifikt assosierte antistoff er sjeldne (se nedenfor), men anti- SSA (Ro 52 eller Ro60) i lave – moderate titere forekommer hos ca. 50% (Wells M, 2022; Cavagna L, 2015).
Historie
Jo-1 antistoffet ble beskrevet første gang i 1980. Sammenheng med Jo-1 antistoffet, lungemanifestasjon og myositt ble beskrevet i 1983. Antisyntetase syndromet benevnes i 1990 (Margurie C, 1990).
Patogenese
Utløsende sykdomsårsak (etiologi) er ukjent, men som ved andre autoimmune sykdommer foreligger redusert evne til å tolerere egne proteiner/vev (autoimmunitet). I patogenesen spiller aminoacyl transfer RNA (tRNA) syntetaser en viktig rolle. Dette er en gruppe intracellulære enzymer som katalyserer tilheftingen av aminosyrer til deres transfer RNA og er essensielle i protein-syntesen. Det finnes en spesifikk aminoacyl tRNA syntetase for hver aminosyre og antistoffene som ses ved ASS (a-Jo-1, a-PL-7, a-PL12 med flere) angriper unike syntetaser (se antistoff nedenfor). Man antar at vevsskader kan fri-sette aminoacyl tRNA fra skadede celler som trigger en kaskade av immunreaksjoner. En direkte patogenetisk betydning av ASS antistoffene er likevel ikke påvist. Genetikk og miljøfaktorer ASS debuterer oftest blant genetisk disponerte personer. HLA DRB1*03:01 forekommer blant 73% av amerikanske pasienter av europeiske avstamning, sammenlignet med 23% hos friske kontroll-personer (O’Hanlon TP, 2006). De kliniske fenotypene / kliniske uttrykksformene kan korrelere med miljø-påvirkning som omfatter antigener via luftveiene: tobakk, vaskemidler (aerosoler, spray), ekskrementer fra fugler, og luft-forurensning. Før antistoff påvises kan symptomene oppfattes som hypersensitivitets pneumoni (Kawano-Dourado L, 2013). CD4 T-celler som er reaktive mot aminoacyl tRNA og anti-Ji-1 antistoff er funnet i bronkial væske ved ASS, noe som også styrker muligheten for at lungene er utgangspunktet for sykdommen (Galindo-Feria AS, 2020).
Epidemiologi

Forekomsten i den generelle befolkningen er ikke godt undersøkt. Orphanet anslår (pr 2023) prevalensen til 1-9/100.000. Gjennomsnittsalder ved debut er 50 år. Kvinner angripes noe oftere enn menn. ASS utgjør opptil 30% av all polymyositt og dermatomyositt.
Symptomer
Sykdomsdebut er ofte hurtig med påvirket allmenntilstand i form av feber, nattesvette og vekttap.
Lungesymptomer kan progrediere raskt eller langsomt. Interstitiell lungesykdom (ILD) er den mest karakteristiske og alvorligste manifestasjon ved ASS. ILD er også den vanligste dødsårsaken. Radiologiske funn og lungefunksjonstester indikerer vanligvis mer alvorlig ILD enn ved andre former for myositt. Utviklingen av ILD er variabel. Omtrent 50% har gradvis progressiv dyspne og tørrhoste, mens den andre halvpart har akutt debut (Tillie-Leblond I, Wislez M, Valeyre D, Crestani B, Rabbat A,, 2008). I den andre enden av spekteret ses noen som oppdages tilfeldig og har nesten ingen progresjon.
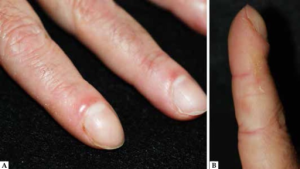
Hud. De mest typiske hud-manifestasjonene (16-21%) er mekaniker-hender som representerer fissurer, hyperkeratotiske og erythematøse forandringer, som ligner hender til mekanikere som belaster hendene fysisk i sitt arbeid. Lokaliseringen er typisk på laterale sider av fingre og tommel og vanligvis ikke i håndflater eller på håndrygg (Hervier B, 2013). “Hikers feet” beskrives som “mekanikerhender” på føtter med hyperkeratose på tær (Trallero-Araguas E, 2016). Hudforandringer som er klassiske for dermatomyositt ses hos ca. 20%, mens mer enn 50% har Raynauds fenomen.

Ledd. Artralgi og artritt i flere ledd, oftest symmetrisk og non-erosiv, ses hos over 50%. Pasienter med anti-Jo-1 antistoff er mest utsatt (Cavagna L 2019). Erosiv artritt ses hos 15-20% av tilfellene. Der polyartritt ses tidlig i sykdomsforløpet foreligger da revmafaktorer og anti-CCP antistoff (Gonzalez-Gay MA, 2018); (Cavagna L, 2010).
Malignitet. Dermatomyositt er assosiert med kreft hos voksne og det er case-rapporter på malignitet også ved ASS. I en større kohorte fant en imidlertid ikke økt malignitet ved ASS sammenlignet med den generelle befolkningen (Pinal-Fernandez I, 2017). Noen pasienter, særlig ved dermatomyositt-lignende forløp eller suspekte symptomer anbefales likevel malignitet-screening.
Muskel. Omtrent en av fire pasienter har få eller ingen tegn til myopati (hypomyopatiske, amyopatiske). Kreatinin kinase (CK) kan være moderat forhøyet eller normal (Cavagna L, 2017: Wells M, 2022).
Utredning
Anamnesen kartlegger symptomer (se ovenfor) med vekt på symptomer fra lunger, muskler (muskelstyrke, øsofagus-funksjon), hud og ledd.
Klinisk undersøkelse. En gjøre en generell status med vekt på vurdering av muskelstyrke, ledd, hud og lunger. Kliniske funn; Artritt. Tre typer: ikke-usurerende med subluksasjon av tomler, ikke-usurende småledds-artritt, destruktiv leddsykdom. Artralgi og artritt i flere ledd, oftest symmetrisk og non-erosiv, ses hos over 50%. Pasienter med anti-Jo-1 antistoff er mest utsatt (Cavagna L 2019). Erosiv artritt ses hos 15-20% av tilfellene.
Feber er ikke spesielt høy. Interstitiell lungesykdom (ILD): Debut av ILD kan være fra asymptomatisk med et tilfeldig funn ved auskultasjon (krepitasjoner). Ved undersøkelse av fingre, særlig pekefinger ses ofte tørr, sprukken hus forenelig med “mekanikerhender” (se foto ovenfor). Myositt trenger ikke være fremtredende eller påvisbar. Raynauds fenomen ses hos mange, men er ofte mindre fremtredende enn ved systemisk sklerose eller MCTD. Sicca symptomer (ofte SSA/anti-Ro antistoffer) kan ses som ved Sjøgrens syndrom, ev. ved overlappende sykdom.
Laboratorieprøver kan omfatte CRP, SR, Hb, leukocytter med differensialtelling, trombocytter, lever-, nyre-, og thyreoidea-funksjonsprøver, elektrolytter, kreatinin kreatin kinase (CK), albumin, glukose. Troponin ved mistanke om myositt. Urin-stiks. I tillegg tas antistoff-prøver som kan omfatte “myositt-spesifikke prøver” (se nedenfor). Der polyartritt ses tidlig i sykdomsforløpet foreligger da revmafaktorer og anti-CCP antistoff (Gonzalez-Gay MA, 2018); (Cavagna L, 2010). Antistoff ved ASS («Myositt-spesifikke antistoff»). 25-30 % av alle pasienter med inflammatorisk myopati/ myositt har anti-syntetase antistoffer som vi kan teste på til nå.
- Jo 1 er rettet mot histidyl tRNA syntetase. vanligst, forekommer hos50-80%. Ofte klassisk antisyntetase syndrom (lunge mer enn 80%, muskler, hud) og leddbetennelser (artritt) hos ca. 70%.
- PL7 mot threonyl tRNA syntetase (Obs! sklerodaktyli, gjerne mild myopati). Ses hos 12-20%, ofte alvorlig lungesykdom, mildere myositt. Raynauds fenomen.
- PL12 mot ananyl tRNA syntetase. Ca. 12-20%, ofte alvorlig lungesykdom, mildere myositt. Raynauds fenomen.
- OJ mot isoleucyl tRNA syntetase. Ca. 5-10%, Mest symptomer fra lunger, sjeldnere myositt. Artritt forekommer.
- EJ mot glycyl tRNA syntetase. Ses hos ca. 4-20%, ofte dermatomyositt, tendens til tilbakefall i sykdomsforløpet.
- KS mot asparaginyl tRNA syntetase (Obs! cancer, kan ha ILD alene). Ca. 5%, Mest lungesykdom, ingen eller mild myositt.
- Zo mot fenylalanin tRNA syntetase forekommer hos færre enn 1%, data for typisk sykdomsforløp mangler.
- Ha/YRS (tyrosyl-tRNA-syntetas), mindre enn 1%, data for typisk sykdomsforløp mangler
- SC (lysyl-tRNA-syntetase), mindre enn 1%, data for typisk sykdomsforløp mangler.
- JS (glutamin-tRNA-syntetase), mindre enn 1%, data for typisk sykdomsforløp mangler
- Tryptophanyl-antistoff, usikker klinisk betydning.
-
Annet: ACPA / CCP-antistoff som ellers forbindes med revmatoid artritt forekommer hos 6-9% med antisyntetase syndrom.
Bildediagnostikk
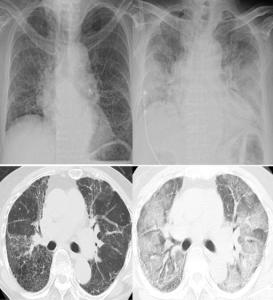
-CT lunger er obligatorisk ved diagnose og i forløpet. Nesten alle (78-100%) klassifiseres som non-spesifikk interstitiell pneumoni (NSIP) med mattglass-forandringer eller organiserende pneumoni (OP). Fibrose og bikake-mønster forenelig som er mer terapiresistent med usual interstitiell sykdom (UIP) kan utvikle seg i forløpet (Waseda Y, 2016).
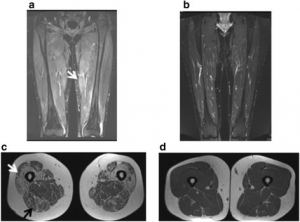
-MR-undersøkelser av lårmuskler kan vise ødem forenelig med myositt og bidra til å lokalisere steder egnet for biopsi. Muskelødem er imidlertid ikke spesifikk for inflammatorisk myopati og ses også ved rabdomyolyse og muskeldystrofi. Ved sykdomsdebut kan også fasciitt observeres (Ebbo M, 2013).
-Røntgen av affiserte ledd (oftest fingre). Erosiv artritt ses hos 15-20% av tilfellene. CT- eller MR av aktuelle organer eller PET/CT dersom mistanke om malignitet.
-Røntgen øsofagus med kontrastmiddel under svelgeakt kan vise om dysmotilitet foreligger.
Lungefunksjonstester viser et restriktivt mønster med nedsatt total lungekapasitet (TLC) <80% av forventet. Gassdiffusjon (DLCO) og funksjonell vital kapasitet (FVC) som ofte følges opp i klinisk praksis er tilsvarende redusert. Både DLCO og FVC korrelerer vanligvis med utbredelsen av ILD slik en ser den ved HRCT (Andersson H, 2016).
Bronkoskopi med bronkial skyllevæske (lavage / BAL) og transbronkial biopsi er invasive undersøkelser som vanligvis ikke er nødvendig ved ASS. Indikasjon foreligger likevel hvis diagnosen er usikker og særlig ved mistanke om infeksjon (pneumocystis og andre opportunistiske), hypersensitivitetspneumoni eller andre differensialdiagnoser. Ved BAL kan lungelegen vurdere parametere som gjenspeiler den inflammatoriske aktiviteten i lungene. I tillegg tas sekret til dyrkning for å utelukke infeksjon (differensialdiagnose).
Elektromyografi (EMG) kan brukes for å styrke mistanken om inflammatorisk myopati. Undersøkelsen skiller mellom muskulær og nevrogen sykdom, men ikke mellom poly- eller dermatomyositt. EMG brukes mindre enn før MR ble mer tilgjengelig.
EKG ved mistanke om hjertemanifestasjon Ekkokardiografi kan gi mistanke om pulmonal hypertensjon som påvises (ved høyresidig hjertekateter) hos 7,9% av pasientene med ASS. Årsaken er vanligvis lungesykdommen ILD, men pulmonal hypertensjon er likevel er uavhengig risikofaktor for alvorlig sykdomsforløp (Hervier B, 2013).
Muskelbiopsi er ikke alltid nødvendig for å stille diagnosen. Imidlertid vil biopsi utelukke lignende tilstander med uspesifikke antistoff-utslag og muskelsmerter. Biopsi kan ofte også skille mellom dermatomyositt og polymyositt. Biopsi ved ASS viser perifascikulær nekrose slik som ved dermatomyositt. Andre funn omfatter nekroser i myofibre utover de perifascikulære områder, samt perimyseal monocellulær celleinfiltrasjon (med opphopning av lymfocytter: B og CD4+ celler). Endomysiale mononukleære infiltrasjoner i ikke-nekrotiske fibre som ses ved polymyositt og inklusjonslegeme-myositt er ikke vanlig (Tanboon J, 2023).
Neglefold-kapillaroskopi. Patologiske funn ses hos over 60%. Disse omfatter periungale teleangiektasier og abnorme neglesengskapillærer. Forandringene er vanligst hos ASS pasienter med Raynauds fenomen, men forekommer også uten Raynauds (Sebastini m, 2019).
6-minutters gangtest. Testen forutsetter at pasienten kan gå minst 6 minutter. Avstanden som tilbakelegges måles og brukes til senere sammenligning. Resultatet preges av en kombinasjon av hjerte- og lungekapasitet, ledd og muskelaffeksjon (Enright PL, 2003).
Klassifikasjonskriterier
ASS kan klassifiseres som en egen diagnose ved siden av polymyositt og dermatomyositt eller inkluderes i disse (Marco JL, 2020).
| Sammenligning av to sett foreslåtte kriterier (Marco JL, 2020) | |
| Absolutt krav: Forekomst av anti-tRNA syntetase antistoff |
|
| Connors GR, 2010 |
Solomon J, 2011 |
| Antisyntetase antistoff pluss ett eller flere av følgende: | Antisyntetase antistoff pluss to major kriterier eller ett major- og to minor kriterier Major kriterier: |
| –Myositt ved Bohan og Peter kriterier (Bohan A, Peter JB. Polymyositis, 1975 del I, del II ) | -Myositt ved Bohan og Peter kriterier (se myositt) |
| –ILD uten annen forklaring eller årsak | -ILD uten annen forklaring eller årsak |
| –Artritt -Uforklart, vedvarende feber -Raynauds fenomen | Minor kriterier: |
| -Mekanikerhender (hud) | -Artritt |
| -Raynauds fenomen | |
| -Mekanikerhender | |
Differensialdiagnoser
Revmatoid artritt. ASS kan initialt bli feildiagnostisert som revmatoid artritt (RA). Dette gjelder særlig når ASS er assosiert med RF eller a-CCP antistoff. Sarkoidose. Uspesifikke utslag i ASS antistoff ved polymyositt eller sarkoidose kan også forveksles med ASS. Sjøgrens syndrom, SLE. Fordi anti-SSA antistoff forekommer er også Sjøgrens syndrom og SLE differensialdiagnoser. Infeksjoner, lungefibrose. Lunge-manifestasjoner blir ofte også feil oppfattet som infeksjoner, hypersensitivitets-pneumoni eller idiopatisk lungefibrose.
Svangerskap
Det er få rapporterte tilfeller av svangerskap ved ASS. Ved alvorlig lungesykdom frarådes oftest svangerskap. Preeklampsi er beskrevet, men uklart om forekomsten er usikkert på grunn av for lite data. Dersom den gravide har SSA antistoff, anbefales oppfølging som ved Sjøgrens syndrom. det innebærer screening av føtal hjertefrekvens i svangerskapsuke 16-26 og vurdering av ev. neonatal lupus etter fødsel (Green LJ, 2020). Vennligst se også info fra NKSR.
Behandling
Sykdomsforløpet ved ASS er individuelt og behandlingen må tilpasses den enkeltes sykdoms-manifestasjoner (persontilpasset behandling), sykdomsforløp, komorbiditet og toleranse. Likevel er noen råd universelle. Blant non-farmakologiske tiltak er fysikalsk behandling, egentrening og i noen tilfeller er lunge-rehabilitering aktuelt. Før en begynner bør en sette mål som skal nås hvis behandlingen virker etter hensikten (“treat to target”). Målet baseres på reduksjon av sykdomsaktivitet og individuelle manifestasjoner.
Valg av medikamenter kan være vanskelig fordi det foreligger relativ få gode studier og ingen medikamenter er spesifikt godkjent for ASS. Dette krever ekstra god pasientinformasjon og oppfølging i henhold til utprøvende behandling. En deler strategien inn i induksjonsbehandling som skal stanse progresjon og redusere inflammasjon, samt en vedlikeholdsbehandling som skal hindre residiv.
Induksjonsbehandling
-Kortikosteroider er viktige i de fleste tilfeller, særlig ved ILD. Dosen baseres på sykdommens alvorlighetsgrad. Ved akutt eller raskt progredierende ILD kan en velge prednisolon 1mg/kg/dag eller metylprednisolon (SoluMedrol) 1000mg/d tre dager på rad (Mimori T, 2012). Lavere doser er aktuelt i mildere sykdomsforløp.
-csDMARDs. Ved ASS assosiert ILD begynnes oftest samtidig med et steroid-sparende DMARD. Mykofenolat (CellCept), azathioprin (Imurel) eller cyklofosfamid (Sendoxan) har alle vanligvis effekt, men mykofenolat ser ut til å ha minst forventede bivirkninger (Huapaya JA, 2019). Calcineurin-hemmere (takrolimus eller ciclosporin) vurderes i behandlingsrefraktære tilfeller (Labirua-Iturburu A, 2013). I utgangspunktet foretrekkes takrolimus på grunn av bedre effekt og mindre risiko for bivirkninger (Witt LJ, 2016).
-Biologisk behandling med rituksimab har vist å kunne bedre og stabilisere ILD ved ASS. Pasienter med sykdomsforløp på under ett år, eksaserbasjoner og de med SSA antistoff ser ut til å respondere best på behandlingen (Sem M, 2009; Bauhammer J, 2016). Imidlertid må en ta hensyn til økt infeksjonsrisiko som være en begrensning i noen tilfeller. Vaksinasjon (influensa, pneumokokker, COVID-19) og profylaktisk behandling mot pneumocystis er aktuelt). I behandlingsrefraktære, alvorlige, progredierende tilfeller kan lungetransplantasjon vurderes (Mimori T, 2012).
Vedlikeholdsbehandling
-csDMARDs. I milde eller moderate tilfeller med myositt velges ofte metotreksat (15-20mg/uke), azathioprin (150mg/d) eller mykofenolat 100-1500 mg to ganger i døgnet) (McGrath ER, 2018). Metotreksat unngås imidlertid ofte ved ILD siden lungebivirkning forekommer (pneumonitt, sjelden) og da kan være vanskelig å skille fra sykdomsprogresjon.
–Biologisk. Rituksimab. Ved alvorligere sykdomsforløp kan mer aggressiv vedlikeholdsbehandling være nødvendig med calcineurin-hemmere eller rituksimab, sjelden cyklofosfamid.
–Immunglobulin intravenøst brukes i sjeldne, behandlingsrefraktære tilfeller eller der annen medikasjon ikke kan brukes (Oddis CV, 2018).
Oppfølging Behandlingen bør ha spesiell fokus på å redusere lunge-infiltrater ved NSIP type. Også undersøkelser i forløpet er viktig fordi 67% som initialt var uten ILD kan utvikle lunge-manifestasjonen i forløpet (Cavagna L, 2015). I oppfølgingen gjøres blant annet lungefunksjons-tester , 6-minutters gangtest, HRCT av lunger. Ved mistanke om pulmonal hypertensjon er ekkokardiografi aktuelt. Muskelstyrken kan vurderes med standardiserte målinger i regi av fysioterapeut.
Prognose
Ved ASS vil en ha størst fokus på å hindre alvorlig progredierende lungesykdom (ILD). En må ved økende dyspne og hoste likevel ikke glemme at pasientene er mottakelige for luftveisinfeksjoner som er hyppige og alvorlige (blant annet ved svelge-besvær og aspirasjon). Dessuten kan progredierende muskulær affeksjon også medføre økende pustebesvær. I en kohorte på 202 pasienter med ASS med anti-Jo-1 antistoff var 5-års overlevelse 90%, 10 års overlevelse 70%. Pasienter uten dette antistoffet hadde mer alvorlig prognose med 5-års overlevelse på 75% og 10 års overlevelse 47%. Vanligste dødsårsak var lungefibrose (Aggarwal R, 2014).
Retningslinjer, anbefalinger, prosedyrer
Litteratur
- Wells M, 2022
- Alfraji N, 2021
- Marco JL, 2020
- Andersson H, 2016
- Trallero-Araguas E, 2016
- Witt LJ, 2016 (behandling)
- Bauhammer J, 2016 (behandling med rituksimab)
