VASKULITT (REV 034-052)
79 ANCA – assosierte vaskulitter, AAV (REV 034)
Ragnar Gunnarsson
GENERELT OM ANCA ASSOSIERT VASKULITT (AAV)
Historikk
Sykdomstilstanden granulomatose med polyangiit (GPA) ble først beskrevet av tyske legestudenten Heinz Klinger ved Charité i Berlin i 1931. Dette ble ytterligere karakterisert av hans venn, Friedrich Wegener, som senere publiserte «Über eine eigenartige rhinogene Granulomatose mit besonderer Beteiligung des Arteriensystem und der Nieren» (Beitr. Path. Anat., 1939). Sykdommen ble først nevnt etter ham Wegeners granulomatose.
Mikroskopisk polyangiit ble første beskrevet av Friedrich Wohlwill i 1923 som «mikroskopisk form» av polyarteritis nodosa.
Eosinofil polyangiit med granulomatose (EPGA) tidligere Churg Strauss syndrom (CSS) ble i 1954 beskrevet av Gabriel Godman og Jacob Churg under definisjonen «microskopic periarteritis».
Klassifikasjon
I 2012 på den internasjonal vaskulitt-konsensus-konferansen som ble avholdt i Chapel Hill i delstaten North Caroline («Chapel Hill Consensus Conference» CHCC 2012) ble sykdomsnavnet Wegeners granulomatose var forandret til granulomatose med polyangiitt (GPA) og Churg Strauss syndrome til eosinofil granulomatose med polyangiit (EGPA) har da definisjonen på MPA og EGPA (1)
Tiende versjon av den internasjonale statistiske klassifikasjonen av sykdommer og beslektede helseproblemer i regi av WHO (ICD10) – M31.3 Granulomatose med polyangiit (GPA), M31.7 Mikroskopisk polyangiitt (MPA) og M30.1 Polyarteritt med lungeaffeksjon / Eosinofil granulomatose med polyangiit (EGPA).
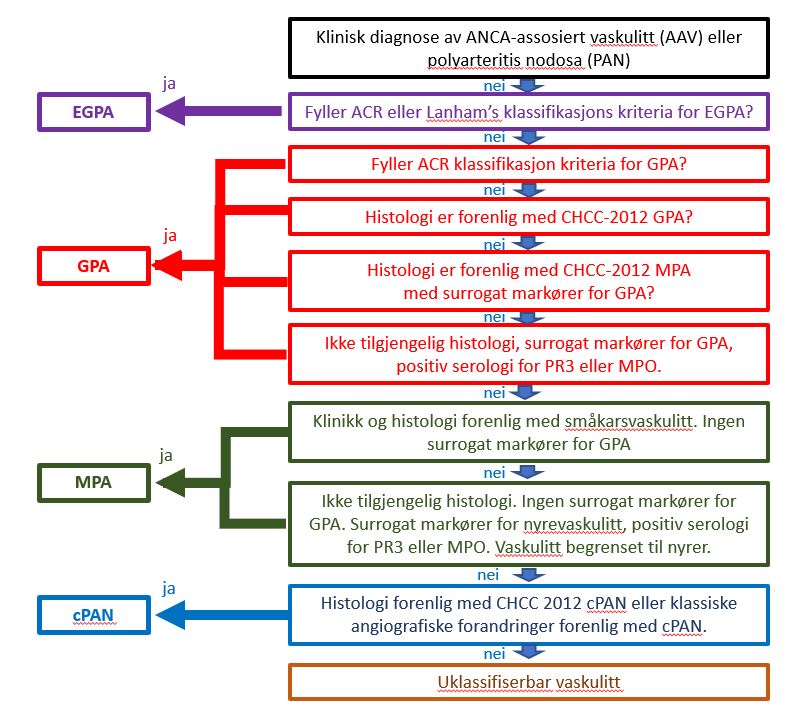
ANCA assosierte vaskulitter (AAV) ble tidligere segregert til EGPA, GPA, MPA og polyarteritis nodosa (PAN) og uklassifisert vaskulitt i forskningsmessig sammenheng ved hjelp av flytskjema algoritme anbefalt bl.a. av European Medicines Agency (EMA) (Figur 1), men dette er nå blitt erstattet med 2022 ACR/EULAR klassikasjonskriteria for GPA, MPA og EGPA (2-5) (Figur 2a-c). Oppdaterte 2022 ACR/EULAR kriteriene inkluderer ANCA titer og har særskilt klassifikasjonskritera for MPA og erstatter 1990 ACR kriteriane for GPA (tidligere Wegeners granulomatosis) og EGPA (Churg-Strauss syndrome) (6-7).
Figur 1. Tidligere foreslått algoritme ved klassifikasjon av ANCA-assosiert vaskulitt og polyarteritis nodosa (2).
ACR: American College of Rheumatology; CHCC-2012 : Chapel Hill Consensus Conference 2012; cPAN : classic polyarteritis nodosa; EGPA : eosinofil granulomatose med polyangiitt; GPA : granulomatose med polyangiitt; MPA : mikroskopisk polyangiitt. MPO : myeloperoksiadase; PR3 : proteinase 3.
Figur 2: 2022 ACR/EULAR klassifikasjonskriteria for:
2a Granulomatose med polyangiitt (GPA) (3).

2b Mikroskopisk polyangiitt (MPA) (4).

2c Eosinofil granulomatose med polyangiitt (EGPA) (5).

Tidligere da man ikke hadde behandling hadde sykdommen GPA var det høy dødelighet. Paradigmeskifte ble når behandling med kortikosteroider og senere cyklofosfamid som ble introdusert i 1973 av Fauci og Wolff på National Institutt of Health (NIH) i USA. Senere paradigmeskiftet kom etter innføring av B-cellerettet anti-CD20 antistoff behandling med rituksimab på 2000 tallet og nå sist komplementhemming med per oral avokopan med kortikosteroid redusert/fri behandling (8).
Definisjon
Vaskulitt er betennelse i blodkarets vegger. Anti-neutrofil cytoplasmatisk antistoffer (ANCA) er assosiert til ANCA assosiert vaskulitt (AAV). AVV påvirker i overveiende grad små kar (dvs. kapillærer, venoler, arterioler og små arterier). Positiv serologi for ANCA har sterk positiv prediktiv verdi for AAV, og som navnet innebær påvises ANCA i over 90% tilfeller. Negativt ANCA utelukker derimot ikke AAV, fordi et mindretall av pasienter med en klinisk og patologisk fenotype som er identisk med ANCA-positiv AAV, er ANCA-negative (dvs. ANCA-negative AAV).
Alvorlig systemisk vaskulitt med livstruende organaffeksjon er sjelden ved negativ ANCA, med viktig unntak av eosinofil granulomatose med polyangiitt (EGPA). Granulomatose med polyangiit (GPA) og mikroskopisk polyangiit (MPA) er på mange måter fenotypisk lik sykdom som blir omhandlet mer her under. Pasienter med negativ AAV har oftest lokal manifestasjoner, men mindre grad av utbredt manifestasjon til tross det kan ramme kritisk unntaket er EPGA.
Den mest informative klassifiseringen og diagnosen AAV inkluderer både den kliniske fenotypen (GPA, MPA, EGPA) og serotypen (PR3-ANCA, MPO-ANCA og ANCA negativ) (1).
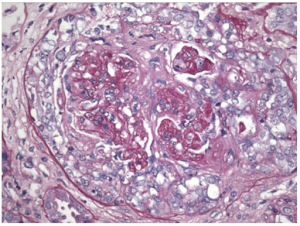
Ved akutt AAV forekommer segmental betennelse med rikelig av nøytrofile leukocytter og nekrose. I løpet av dager og/eller uker utvikler dette seg til lesjoner med kronisk inflammasjon med overvekt av lymfocytter og monocytter, og etter hvert fibrose. I en biopsi kan man oftest se forskjellige faser av denne utviklingen. AAV er en nekrotiserende vaskulitt med få eller ingen immunavsetninger (pauciimmun). Pauciimmun vaskulitt karakteriseres med å ha få eller ingen immunavsetninger av immunglobulin og komplement i karvegger, som skiller AAV fra immunkompleks vaskulitt og anti-glomerulær basalmembranantistoff (anti-GBM) mediert vaskulitt (Goodpasture sykdom). Imidlertid utelukker ikke immunhistologisk identifikasjon av moderat til markerte karveggavsetninger av immunglobulin og/eller komplement-fraksjoner AAV. AAV kan i svært sjeldne tilfeller opptre samtidig med anti-GBM sykdom eller immunkompleks sykdom.
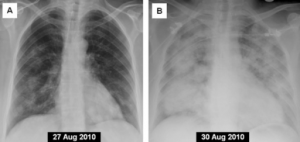
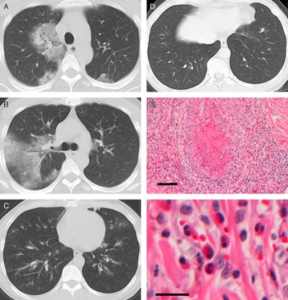
Symptomer og funn som er assosiert til AAV inkluderer; allmennsymptomer, vekttap, leddsmerter og artritt, hudpurpura, petekkier, ulcera, glomerulonefritt med mikroskopisk hematuri, erytrocytt sylinderuri og/eller proteinuri, og nyresvikt. Radiografisk konsolideringer i lunger, dyspne, hemoptyse, lungeblødning og lungefibrose. Episkleritt, okulær skleritt, uveitt eller ulcerøs keratitt. Nesetetthet, epistaxis, «sadelnese» bihuleaffeksjon med destruksjoner og bennydannelse, mastoiditt, otitt og hørselstap. Astma, eosinofili, hjerteaffeksjon med hjertesvikt og/eller ledningsforstyrrelser, mononevritis multipleks og polynevropati.
Ytterligere litteratur
- Kronbichler, A., et al. (2024). “Diagnosis and management of ANCA-associated vasculitis.” Lancet 403(10427): 683-698.
- Hellmich, B., et al. (2024). “EULAR recommendations for the management of ANCA-associated vasculitis: 2022 update.” Ann Rheum Dis 83(1): 30-47.
- Kitching, A. R., et al. (2020). “ANCA-associated vasculitis.” Nat Rev Dis Primers 6(1): 71.
- Trivioli, G., et al. (2022). “Genetics of ANCA-associated vasculitis: role in pathogenesis, classification and management.” Nat Rev Rheumatol 18(10): 559-574.
Referanser
- Jennette JC, Falk RJ, Bacon PA, Basu N, Cid MC, Ferrario F, et al. 2012 Revised International Chapel Hill Consensus Conference Nomenclature of Vasculitides. Arthritis & Rheumatism. 2013;65(1):1-11.
- Watts R, Lane S, Hanslik T, Hauser T, Hellmich B, Koldingsnes W, et al. Development and validation of a consensus methodology for the classification of the ANCA-associated vasculitides and polyarteritis nodosa for epidemiological studies. Ann Rheum Dis. 2007;66(2):222-7
- Robson JC, Grayson PC, Ponte C, Suppiah R, Craven A, Judge A, et al. 2022 American College of Rheumatology/European Alliance of Associations for Rheumatology classification criteria for granulomatosis with polyangiitis. Ann Rheum Dis. 2022;81(3):315-20.
- Suppiah R, Robson JC, Grayson PC, Ponte C, Craven A, Khalid S, et al. 2022 American College of Rheumatology/European Alliance of Associations for Rheumatology classification criteria for microscopic polyangiitis. Ann Rheum Dis. 2022;81(3):321-6
- Grayson PC, Ponte C, Suppiah R, Robson JC, Craven A, Judge A, et al. 2022 American College of Rheumatology/European Alliance of Associations for Rheumatology Classification Criteria for Eosinophilic Granulomatosis with Polyangiitis. Ann Rheum Dis. 2022;81(3):309-14.
- Leavitt RY, Fauci AS, Bloch DA, Michel BA, Hunder GG, Arend WP, et al. The American College of Rheumatology 1990 criteria for the classification of Wegener’s granulomatosis. Arthritis Rheum. 1990;33(8):1101-7.
- Masi AT, Hunder GG, Lie JT, Michel BA, Bloch DA, Arend WP, et al. The American College of Rheumatology 1990 criteria for the classification of Churg-Strauss syndrome (allergic granulomatosis and angiitis). Arthritis Rheum. 1990;33(8):1094-100.
- Jayne DRW, Merkel PA, Schall TJ, Bekker P, Group AS. Avacopan for the Treatment of ANCA-Associated Vasculitis. The New England journal of medicine. 2021;384(7):599-609.
